
下列叙述正确的是( )
|
| A. | 非金属元素的原子最外层电子数都大于或等于4 |
|
| B. | 只有非金属能形成含氧酸或含氧酸盐 |
|
| C. | Na2O2中阴阳离子的个数比为1:1 |
|
| D. | 非金属元素组成的化合物不一定是共价化合物 |
考点:
共价键的形成及共价键的主要类型;原子核外电子排布;离子化合物的结构特征与性质.
分析:
A.H为非金属性元素,原子核外最外层电子数为1;
B.金属性较弱的金属可形成含氧酸盐;
C.Na2O2晶体中阳离子为Na+、阴离子为O22﹣;
D.非金属元素也能形成离子化合物.
解答:
解:A.H为非金属性元素,原子核外最外层电子数为1,He最外层为2,故A错误;
B.金属性较弱的金属可形成含氧酸盐,如高锰酸钾、偏铝酸钠等,故B错误;
C.Na2O2晶体中阳离子为Na+、阴离子为O22﹣,所以Na2O2晶体中阴阳离子个数之比为1:2,故C错误;
D.非金属元素组成的化合物可能为离子化合物,如硝酸铵、氯化铵等,故D正确.
故选D.
点评:
本题考查元素周期律和周期表、以及化学键的有关知识,侧重于学生的分析能力的考查,注意把握元素周期律的递变规律,把握物质的性质的判断角度,难度不大.


 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
肯定属于同族元素且性质相似的是( )
|
| A. | 原子核外电子排布式:A为1s22s2,B为1s2 |
|
| B. | 结构示意图:A为 |
|
| C. | A原子基态时2p轨道上有1个未成对电子,B原子基态时3p轨道上也有1个未成对电子 |
|
| D. | A原子基态时2p轨道上有一对成对电子,B原子基态时3p轨道上也有一对成对电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
对于某些离子的检验及结论一定正确的是( )
|
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32﹣ |
|
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42﹣ |
|
| C. | 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ |
|
| D. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
正确掌握化学用语和化学基本概念是学好化学的基础.下列有关表述中正确的一组是( )
|
| A. | 16O与18O互为同位素;H2 |
|
| B. | SiH4、PH3、HCl的稳定性逐渐增强 |
|
| C. | 氧化铁的化学式:FeO |
|
| D. | Ca2+的结构示意图为 |
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z的原子序数依次增大,Y为IA族元素,X与Z同主族,3种元素原子的最外层电子数之和为13.下列判断正确的是( )
|
| A. | Y元素位于第2周期 |
|
| B. | Y、Z均能与X形成不只一种化合物 |
|
| C. | X是ⅤA族元素 |
|
| D. | 氢化物的稳定性:HnZ>HnX |
查看答案和解析>>
科目:高中化学 来源: 题型:
几种短周期元素的原子半径和主要化合价见表,下列有关说法中,正确的是( )
| 元素代号 | X | Y | Z | L | M | Q |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.112 | 0.074 |
| 主要化合价 | +2 | +3 | +6、﹣2 | +7、﹣1 | +2 | ﹣2 |
|
| A. | 等物质的量的X、Y的单质与足量盐酸反应,生成H2一样多 |
|
| B. | Y与Q形成的化合物不可能跟氢氧化钠溶液反应 |
|
| C. | Z的氢化物的稳定性强于L的氢化物的稳定性 |
|
| D. | 与稀盐酸反应的剧烈程度:M单质<X单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用铝土矿 (主要成分为Al2O3、Fe2O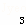 、SiO2)提取氧化铝做冶炼铝的原料,提取的操作过程如下:
、SiO2)提取氧化铝做冶炼铝的原料,提取的操作过程如下: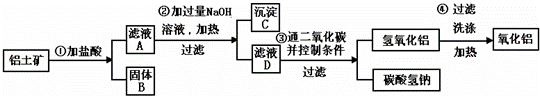
(1)第一步在铝土矿中加入盐酸后的实验基本操作是 ,若在固体B中加入氢氧化钠溶液 会 (填”会”或”不会”)发生反应,若会,则写出反应的离子方程式 S
(2)验证滤液A中是否含Fe3+,可取少量滤液A并加入 (填试剂化学式),现象是 .
(3)在整个操作过程中 (填“是”“否”)有氧化还原反应;写出碳酸氢钠的一种用 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | 含有双键的物质是烯烃 |
|
| B. | 能使溴水褪色的物质是烯烃 |
|
| C. | 分子式为C4H8的链烃一定是烯烃 |
|
| D. | 分子中所有原子在同一平面的烃是烯烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在完全满足可逆反应:2H2O(g)⇌2H2+O2,2CO+O2⇌2CO2能顺利进行的条件下,将2molH2O(g)和2molCO充入1L密闭容器中,使其发生反应.
(1)当上述两个反应达到平衡时,至少要知道两种气体的平衡浓度才能计算出平衡时混合物的组成,但这两种气体不能同时是 和 ,或 和 (填它们的分子式).
(2)若平衡时,O2和CO2的物质的量分别为amol和bmol,则n(H2O)平为 mol (用含a、b的代数式表示).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com