
【题目】下列离子方程式正确的是
A. 氯气溶于水:Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
B. 钠与水反应:Na+2H2O===Na+2OH+H2↑
C. 氧化亚铁溶于稀硝酸:FeO+2H+===Fe2++H2 O
D. 向碳酸氢铵溶液中加入足量石灰水:NH4++HCO3-+Ca2++2OH-===CaCO3 ↓+NH3·H2O+H2O
 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
【题目】利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如下图所示:
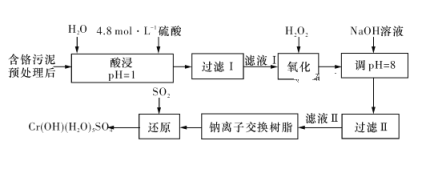
其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(1)实验室用18.4 mol·L-1的浓硫酸配制240 mL 4.8 mol·L-1的硫酸溶液,需量取浓硫酸__________mL;配制时所用玻璃仪器除量筒、烧杯、胶头滴管和玻璃棒外,还需____________。
(2)“酸浸”时,为了提高浸取率可采取的措施有__________________。
(3)H2O2的作用是将“滤液Ⅰ”中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:___________________。
(4)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下表所示:
阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
开始沉淀时的pH | 2.7 | — | — | — |
沉淀完全时的pH | 3.7 | 11.1 | 5.4(>8溶解) | 9(>9溶解) |
加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-。过滤后“滤液Ⅱ”中的阳离子主要有Na+、Ca2+、Mg2+,但溶液的pH不能超过8,其理由是__________________。
(5)钠离子交换树脂的反应原理为Mn++nNaR===MRn+nNa+,利用钠离子交换树脂除去“滤液Ⅱ”中的金属阳离子是________(填离子符号)。
(6)写出上述流程中用SO2进行还原时发生反应的化学方程式:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 同温同压下甲烷和氧气的密度之比为2∶1
B. 1 g甲烷和1 g氧气的原子数之比为5∶1
C. 等物质的量的甲烷和氧气的质量之比为2∶1
D. 在标准状况下等质量的甲烷和氧气的体积之比为1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是
A. 在1 L0.1 mol/L的硫化钠溶液中,阴离子总数大于0.1NA
B. 常温常压下,Na2O2与足量H2O反应,生成4.48LO2,转移电子的数目为0.2NA
C. 在密闭容器中充入1.5 mol H2和0.5 mol N2,充分反应后可得到NH3的分子数为NA
D. 电解精炼铜的过程中,电路中每通过NA个电子,阳极溶解铜32g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 实验室用大理石和稀盐酸制取CO2:2H++CO![]() ===CO2↑+H2O
===CO2↑+H2O
B. 碳酸氢钠与烧碱溶液反应:H++CO![]() +OH-===CO
+OH-===CO![]() +H2O
+H2O
C. 硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO![]() ===BaSO4↓
===BaSO4↓
D. 醋酸跟KOH溶液反应:CH3COOH+OH-===CH3COO-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将质量为1.15 g钠用刺了孔的铝箔包裹后放入水中,共收集到1.232 L(标准状况)气体。请回答下列问题:
(1)1.15 g钠与水反应,理论上生成气体的体积(标准状况)为__________ L 。
(2)Al和NaOH溶液反应也能生成H2,写出相应的化学方程式:_____________;
(3)若反应后溶液的体积为100 mL,则溶液中NaOH的物质的量浓度为多少?(写出计算过程)_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下;用惰性电极电解200 mL NaCl、CuSO4的混合溶液;阴、阳两极所得气体的体积随时间变化如图所示;则 c(CuSO4)为
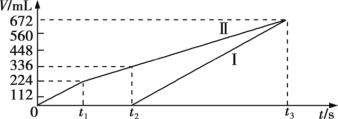
A. 0.10 mol·L1 B. 0.15 mol·L1 C. 0.20 mol·L1 D. 0.25 mol·L1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟他胺G是一种可用于治疗肿瘤的药物。实验室由芳香烃A制备G的合成路线如下:
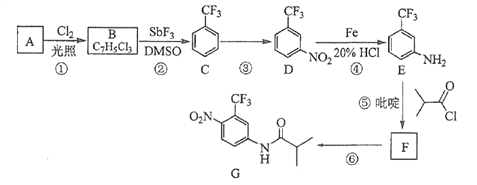
回答下列问题:
(1)A的结构简式为____________。C的化学名称是______________。
(2)③的反应试剂和反应条件分别是____________________,该反应的类型是__________。
(3)⑤的反应方程式为_______________。吡啶是一种有机碱,其作用是____________。
(4)G的分子式为______________。
(5)H是G的同分异构体,其苯环上的取代基与G的相同但位置不同,则H可能的结构有______种。
(6)4-甲氧基乙酰苯胺(![]() )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚(![]() )制备4-甲氧基乙酰苯胺的合成路线___________(其他试剂任选)。
)制备4-甲氧基乙酰苯胺的合成路线___________(其他试剂任选)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com