
【题目】室温时,向20mL0.1mol/L的醋酸溶液中不断滴入0.1mol/L的NaOH溶液,溶液的pH变化曲线如图所示.下列说法中正确的是
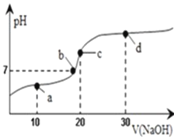
A.a点时:c(CH3COO-)c(Na+)c(H+)c(OH-)
B.用甲基橙试液作指示剂时终点颜色变化是由红色变为橙色
C.c点时:c(H+)=c(OH-)+c(CH3COOH)
D.d点时:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
【答案】A
【解析】
A. a点溶质为醋酸和醋酸钠且两者浓度相等,溶液显酸性,醋酸的电离程度大于醋酸钠的水解程度,因此离子浓度大小关系为:c(CH3COO-)>c(Na+) >c(H+) >c(OH-),故A正确;
B. 两者恰好完全反应时溶液显碱性,应选用酚酞试液作指示剂,终点现象是溶液由无色变为浅红色、且30s内不褪去,故B错误;
C. c点溶质为醋酸钠,醋酸根水解溶液显碱性,溶液中质子守恒为c(OH-) = c(H+)+c(CH3COOH),故C错误;
D. d点为醋酸钠和氢氧化钠且浓度之比为2:1,溶液呈碱性,醋酸根离子的水解程度是微弱的,因此离子浓度大小关系为:c(Na+) >c(CH3COO-)>c(OH-)>c(H+),故D错误;
综上所述,答案为A。


科目:高中化学 来源: 题型:
【题目】下列各组数据中,后者刚好是前者两倍的是
A.51 g氧化铝中氧原子数和67.2 L一氧化碳中氧原子数
B.1molCO2的摩尔质量和2 molCO2的摩尔质量
C.50 mL 2 mol·L-1氯化钠溶液中c(Cl-)和50 mL 2 mol·L-1氯化镁溶液中c(Cl-)
D.1molNa2O2固体中阳离子与阴离子比值和1molNa2O固体中阳离子与阴离子比值
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某地海水中主要离子的含量如下表,现利用“电渗析法”进行淡化,技术原理如图所示(两端为惰性电极,阳膜只允许阳离子通过,阴膜只允许阴离子通过)。下列有关说法错误的是
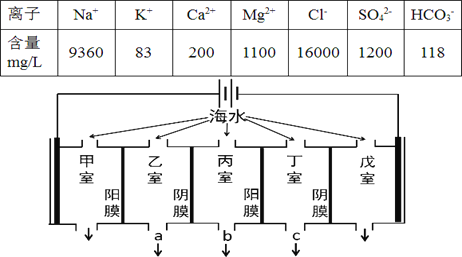
A. 甲室的电极反应式为:2Cl--2e-= Cl2↑
B. 淡化过程中易在戊室形成水垢
C. 乙室和丁室中部分离子的浓度增大,淡水的出口为 b
D. 当戊室收集到22.4L(标准状况)气体时,通过甲室阳膜的离子的物质的量一定为2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多晶硅是制作光伏电池的关键材料。以下是由粗硅制备多晶硅的简易过程。
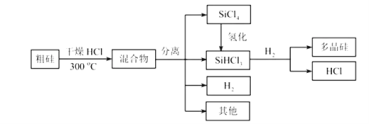
回答下列问题:
(I)硅粉与HCl在300℃时反应生成1mol SiHCl3气体和![]() ,放出225kJ热量,该反应的热化学方程式为________________________。
,放出225kJ热量,该反应的热化学方程式为________________________。![]() 的电子式为__________________。
的电子式为__________________。
(II)将![]() 氢化为
氢化为![]() 有三种方法,对应的反应依次为:
有三种方法,对应的反应依次为:
①SiCl4(g)+H2(g)![]() SiHCl3(g)+HCl(g)△H1>0
SiHCl3(g)+HCl(g)△H1>0
②3SiCl4(g)+2H2(g)+Si(s)![]() 4SiHCl3(g) △H2>0
4SiHCl3(g) △H2>0
③3SiCl4(g)+H2(g)+Si(s)+HCl(g)![]() 3SiHCl3△H3
3SiHCl3△H3
反应③的![]() ______(用△H1,△H2表示)。温度升高,反应③的平衡常数K______(填“增大”、“减小”或“不变”)。
______(用△H1,△H2表示)。温度升高,反应③的平衡常数K______(填“增大”、“减小”或“不变”)。
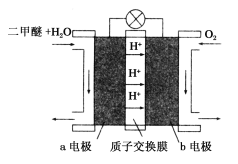
(III)如图为绿色电源“二甲醚(CH3OCH3)燃料电池”的工作原理示意图.b电极是________极。请写出负极的电极反应方程式:__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲胺(CH3NH2)是一种一元弱碱,其电离方程式为:CH3NH2 + H2O ![]() CH3NH3+ + OH-。常温下,向20.0 mL 0.10 mol/L的甲胺溶液中滴加VmL0.10mol/L的稀盐酸,混合溶液的pH与相关微粒浓度的关系如图所示。下列说法中错误的是
CH3NH3+ + OH-。常温下,向20.0 mL 0.10 mol/L的甲胺溶液中滴加VmL0.10mol/L的稀盐酸,混合溶液的pH与相关微粒浓度的关系如图所示。下列说法中错误的是

A. b点对应加入盐酸的体积V<20.00mL
B. 常温下,根据a点可知甲胺的电离平衡常数Kb=10 -3.4
C. b点可能存在关系:c(Cl-) > c(CH3NH3+) > c(H+) = c(OH-)
D. V=20.00mL时,溶液呈弱酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=1的两种酸溶液HA、HB各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图所示,下列说法不正确的是
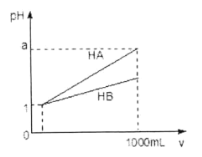
A. 同浓度、同体积的HA、HB溶液分别加入过量的锌粒,产生的氢气体积后者大
B. 物质的量浓度HA<HB
C. 若1<a<4,则HA、HB都是弱酸
D. 体积相同pH均为1的HA、HB溶液分别滴加同浓度的NaOH溶液至中性,前者消耗的NaOH少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃、101KPa时,agNH3与bgCH4的体积相同,下列叙述不正确的是
A.NH3、CH4的物质的量之比为a: b
B.NH3、CH4两种气体的密度之比为a: b
C.NH3、CH4的摩尔质量之比为17: 16
D.NH3、CH4的分子数之比为1 : 1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】秸秆(含多糖物质)的综合应用具有重要的意义。下面是以秸秆为原料合成聚酯类高分子化合物的路线:

回答下列问题:
(1)下列关于糖类的说法正确的是______________。(填标号)
a.糖类都有甜味,具有CnH2mOm的通式
b.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
c.用银镜反应不能判断淀粉水解是否完全
d.淀粉和纤维素都属于多糖类天然高分子化合物
(2)B生成C的反应类型为______。
(3)D中官能团名称为______,D生成E的反应类型为______。
(4)F 的化学名称是______,由F生成G的化学方程式为______。
(5)具有一种官能团的二取代芳香化合物W是E的同分异构体,0.5 mol W与足量碳酸氢钠溶液反应生成44 gCO2,W共有______种(不含立体结构),其中核磁共振氢谱为三组峰的结构简式为_________。
(6)参照上述合成路线,以(反,反)-2,4-己二烯和C2H4为原料(无机试剂任选),设计制备对二苯二甲酸的合成路线_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com