
下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
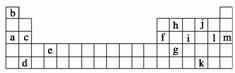
(1)下列________(填写编号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、l ④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响:
A.原子核对核外电子的吸引力
B.形成稳定结构的倾向
下表是一些气态原子核失去核外不同电子所需的能量(kJ·mol-1):
| 锂 | X | Y | |
| 失去第一个电子 | 519 | 502 | 580 |
| 失去第二个电子 | 7 296 | 4 570 | 1 820 |
| 失去第三个电子 | 11 799 | 6 920 | 2 750 |
| 失去第四个电子 | 9 550 | 11 600 |
①通过上述信息和表中的数据分析,为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量__________________________________________
________________________________________________________________________。
②表中X可能为以上13种元素中的________(填写字母)元素。用元素符号表示X和j形成的化合物的化学式____________________。
③Y是周期表中________族元素。
④以上13种元素中,________(填写字母)元素原子失去核外第一个电子需要的能量最多。
科目:高中化学 来源: 题型:
某化合物的分子式为AB2,A属ⅥA族元素,B属ⅦA族元素,A和B在同一周期,它们的电负性值分别为3.44和3.98,已知AB2分子的键角为103.3°。下列推断不正确的是( )
A.AB2分子的空间构型为“V”形
B.A-B键为极性共价键,AB2分子为非极性分子
C.AB2与H2O相比,AB2的熔点、沸点比H2O的低
D.AB2分子中无氢原子,分子间不能形成氢键,而H2O分子间能形成氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
当前环境污染问题越来越严重,如酸雨、温室效应、臭氧层破坏、有毒物质的污染、汽车尾气的污染、水体污染等已成为世界各国普遍关注和研究的问题。
请回答:
(1)引起温酸雨的主要气体是 (填序号,下同)。
①SO2 ②CO2
(2)使臭氧层受到破坏的主要气体是 。
①二氧化碳 ②氟氯代烷
(3)造成居室污染的物质是 。
①CO ②N2
(4)造成水体污染的原因是 。
①生活污水的任意排放 ②工业废水的任意排放
(5)为了治理汽车污染问题,可以在汽车的排气管上装一个“催化转化器”(用铂、钯合金作催化剂)。它特点是使汽车排放出的CO与NO反应,生成CO2和N2,写出该反应的化学方程式: 。
(6)煤的气化可有效地降低大气中污染物的排放,是高效、清洁的利用煤炭的重要途径。一些城市中使用的水煤气是将焦炭与水蒸气在高温下反应得到的,该反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构。下列推测不正确的是( )
A.同周期元素中X的金属性最强
B.原子半径X>Y,离子半径X+>Z2-
C.同族元素中Z的氢化物稳定性最高
D.同周期元素中Y的最高价含氧酸的酸性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
日本福岛第一核电站发生严重的核辐射泄漏,日本政府向核电站附近居民发放碘片( 127I),以降低放射性碘对人体的伤害。已知放射性碘(131I)的核电荷数为 53,则下列说法正确的是( )
A.127I与131I互为同素异形体 B. 131I和131Xe互为同位素
C.131I 原子的中子数为78 D.127I 原子和131I 原子的相对原子质量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的性质比较,正确的是( )
A.酸性:H2SO4>HClO4>HBrO4 B.碱性:NaOH>KOH>RbOH
C.非金属性: P>S>Cl D.气态氢化物稳定性:HF>H2O>PH3
查看答案和解析>>
科目:高中化学 来源: 题型:
丙烯酰胺(H2C===CH—CONH2)具有中等毒性,它对人体可造成神经毒性和遗传毒性。丙烯酰胺主要是由高碳水化合物、低蛋白质的植物性食物在加热(120 ℃以上)烹调过程中形成,特别在烘烤、油炸时更易形成。丙烯酰胺可以进一步形成在工业上有用的聚丙烯酰胺类物质。
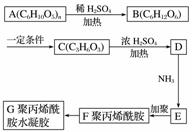
回答下列问题:
(1)D的结构简式为________________,F的结构简式为______________。
(2)指明下列反应类型:
A—→B____________,C—→D____________。
(3)丙烯酰胺有多种同分异构体,写出分子中同时含有醛基和碳碳双键的同分异构体:________________________________________________________________________。
(4)写出D—→E的化学方程式:_____________________________________________。
2分子C在浓硫酸作用下可形成一个六元酯环,该反应的化学方程式为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com