
| 电离能(KJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15399 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
 .
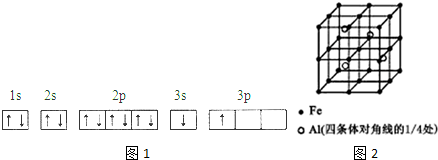
.分析 (1)①由图1电子轨道排布图可知,3s能级未填满就填充3p能级,3s能级能量比3p能级低,每个轨道最多只能容纳两个电子,且自旋相反;
由表中电离能可知,二者第三电离能剧增,故为+2价,都为短周期元素,故A为铍、B为Mg,镁价层电子排布为3s2;
②BeCl2分子中Be的成2个σ键,杂化轨道数为2,采取sp杂化,没有孤对电子对,为直线型;
(2)①体心立方堆积,如: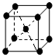 ,属于钾、钠和铁型,其原子的配位数为8;
,属于钾、钠和铁型,其原子的配位数为8;
②等电子体中原子个数相等、价电子数相等,CN-含有2个原子、价电子数是10,与单质氮气分子是等电子体关系;
③六氰合亚铁离子[Fe(CN)6]4-中存在配位键,极性共价键,CN-电子式为 ,则C、N间存在σ键和π键;
,则C、N间存在σ键和π键;
(3)①由晶胞图2,晶胞中含有4个Al原子,且都位于晶胞内部,则晶胞平均含有4个Al,晶胞中Fe位于顶点的有8个,位于面心的有6个,位于棱上的有12个,位于体心的有1个,根据均摊法计算;
②一个晶胞中含有8个Fe原子和4个Al原子,合金中最近的两个Fe原子之间的距离为xcm,则棱长为2xcm,体积为8x3cm3,晶胞质量为$\frac{56×8+27×4}{{N}_{A}}$g,结合ρ=$\frac{m}{V}$计算.
解答 解:(1)①由图1电子轨道排布图可知,3s能级未填满就填充3p能级,所以违背能量最低原理;由表中电离能可知,二者第三电离能剧增,故为+2价,都为短周期元素,故A为铍、B为Mg,镁价层电子排布为3s2,处于周期表中s区,
故答案为:能量最低原理;s;
②BeCl2分子中Be的成2个σ键,杂化轨道数为2,采取sp杂化,没有孤对电子对,为直线型,故答案为:sp;直线形;
(2)①体心立方堆积,如: ,属于钾、钠和铁型,其原子的配位数为8,故答案为:8;
,属于钾、钠和铁型,其原子的配位数为8,故答案为:8;
②等电子体中原子个数相等、价电子数相等,CN-含有2个原子、价电子数是10,与单质氮气分子是等电子体关系,氮气的电子式为 ,
,
故答案为: ;
;
③六氰合亚铁离子[Fe(CN)6]4-中存在配位键,极性共价键,CN-电子式为 ,则C、N间存在σ键和π键,
,则C、N间存在σ键和π键,
故答案为:B;
(3)①由晶胞图2,晶胞中含有4个Al原子,且都位于晶胞内部,则晶胞平均含有4个Al,晶胞中Fe位于顶点的有8个,位于面心的有6个,位于棱上的有12个,位于体心的有1个,含有Fe原子数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$+12×$\frac{1}{4}$+1=8,Fe与 Al原子数目之比为8:4=2:1,故该合金的化学式为Fe2Al,故答案为:Fe2Al;
②一个晶胞中含有8个Fe原子和4个Al原子,设合金中最近的两个Fe原子之间的距离为xcm,则棱长为2xcm,体积为8x3cm3,晶胞质量为$\frac{56×8+27×4}{{N}_{A}}$g,由ρ=$\frac{m}{V}$可知,8x3=$\frac{139}{ρ{N}_{A}}$,则x=$\root{3}{\frac{139}{2ρ{N}_{A}}}$cm,故答案为:$\root{3}{\frac{139}{2ρ{N}_{A}}}$.
点评 本题考查物质结构和性质,为高频考点,侧重对物质结构主干知识的考查,涉及杂化理论、化学键、分子结构与性质、晶胞计算等,需要学生具备知识的基础,题目难度中等,注意对晶胞计算中的常用的均摊法的理解及应用.


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:选择题
| A. | 有单质生成的反应一定是氧化还原反应 | |
| B. | 在氧化还原反应中,非金属单质一定是氧化剂 | |
| C. | 反应前后有元素化合价变化的反应一定是氧化还原反应 | |
| D. | 金属阳离子被还原一定得到金属单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
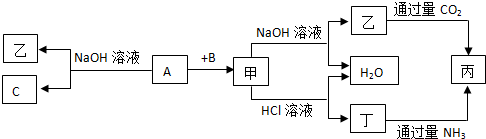
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用水鉴别炭粉和二氧化锰 | |
| B. | 用闻气味的方法鉴别白酒和白醋 | |
| C. | 用澄清石灰水鉴别氮气和二氧化碳 | |
| D. | 用相互刻画的方法鉴别黄铜片和铜片 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
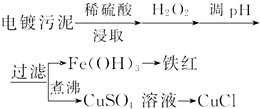
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 2.3 | 7.6 | 4.4 |
| 完全沉淀的pH | 3.2 | 9.7 | 6.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com