
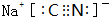 .
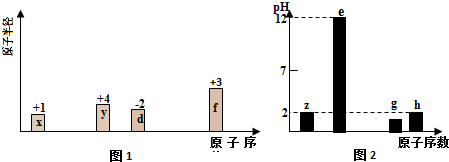
. 分析 从图中的化合价、原子半径的大小及原子序数,可知x是H元素,y是C元素,z是N元素,d是O元素,f是Al元素,z、e、g、h的最高价氧化物对应水化物溶液浓度均为0.01mol•L-1,e的pH为12,为一元强碱,则e是Na元素,z、h的pH均为2,为一元强酸,则z为N元素、h为Cl元素;g的pH小于2,则g的为二元强酸,故g为S元素.
(1)主族元素周期数=电子层数、主族族序数=最外层电子数;
(2)电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大;
金属性越强,最高价氧化物水化物的碱性越强;
(3)a.单质的硬度和熔、沸点,属于物理性质,不能比较金属强弱;
b.溶液pH越小,水解程度越大,对应元素的金属性越弱;
c.金属性越强,单质与同浓度盐酸反应越剧烈;
d.金属性强弱与失去电子数目无关,与得失电子难易有关;
(4)任三种组成六原子共价化合物有HClO4、H2CO3、H2SO3等;
(5)N4气体转变为N2气体先破坏N4分子N-N键吸收能量,再生成N2分子形成N≡N键放出能量,注意一个N4分子中含有6个N-N键,计算能量的变化,注明聚集状态、反应热书写热化学方程式;
(6)化合物NaCN不慎泄露时,通常采用喷洒过氧化氢溶液的方式处理,以较少污染.反应生成一种酸式盐和一种气体,二者溶于水均呈碱性,应生成NaHCO3、NH3;
NaCN由Na+、CN-构成,含有N2分子中类似的化学键,则CN-中存在三键.
解答 解:从图中的化合价、原子半径的大小及原子序数,可知x是H元素,y是C元素,z是N元素,d是O元素,f是Al元素,z、e、g、h的最高价氧化物对应水化物溶液浓度均为0.01mol•L-1,e的pH为12,为一元强碱,则e是Na元素,z、h的pH均为2,为一元强酸,则z为N元素、h为Cl元素;g的pH小于2,则g的为二元强酸,故g为S元素.
(1)h为Cl元素,处于周期表中第三周期第ⅦA族,故答案为:第三周期第ⅦA族;
(2)电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大,则离子半径:S2->Cl->Al3+;
金属性Na>Al,金属性越强,最高价氧化物水化物的碱性越强,故金属性NaOH>Al(OH)3,
故答案为:S2->Cl->Al3+;NaOH;
(3)a.单质的硬度和熔、沸点,属于物理性质,不能比较金属强弱,故A错误;
b.溶液pH越小,金属阳离子水解程度越大,金属阳离子对应的键越弱,则对应元素的金属性越弱,故b正确;
c.单质与同浓度盐酸反应越剧烈,说明金属性越强,故c正确;
d.化合物中金属元素化合价越高,说明金属原子失去电子越大,但金属性强弱与失去电子数目无关,与得失电子难易有关,故d错误,
故选:bc;
(4)任三种组成六原子共价化合物有HClO4、H2CO3、H2SO3等,
故答案为:HClO4、H2CO3、H2SO3等;
(5)根据原子守恒知,一个N4分子生成2个N2分子,一个N4分子中含有6个N-N键,破坏1molN4分子中含有6molN-N键需要吸收167kJ/mol×6mol=1002kJ能量;
生成2molN≡N键放出942kJ/mol×2mol=1884kJ能量,所以该反应放出1884kJ-1002kJ=882kJ能量,所以热化学反应方程式为N4(g)=2N2(g)△H=-882kJ/mol,
故答案为:N4(g)=2N2(g)△H=-882kJ/mol;
(6)化合物NaCN不慎泄露时,通常采用喷洒过氧化氢溶液的方式处理,以较少污染.反应生成一种酸式盐和一种气体,二者溶于水均呈碱性,应生成NaHCO3、NH3,反应方程式为:NaCN+H2O2+H2O=NaHCO3+NH3↑,
NaCN由Na+、CN-构成,含有N2分子中类似的化学键,则CN-中存在三键,NaCN电子式为: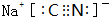 ,
,
故答案为:NaCN+H2O2+H2O=NaHCO3+NH3↑;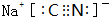 .
.
点评 本题考查结构位置性质关系、半径的大小比较、元素周期律、热化学方程式书写、盐类水解等,是对学生综合能力的考查,需要学生具备扎实的基础,难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | Na与水反应 Na+2H2O═Na++2OH-+H2↑ | |
| B. | 向AlCl3溶液中加入过量的NaOH溶液 Al3++3OH-═Al(OH)3↓ | |
| C. | 氢氧化钡溶液与硫酸溶液反应 Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | CO2通入过量澄清石灰水 CO2+Ca2++2OH-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
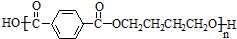
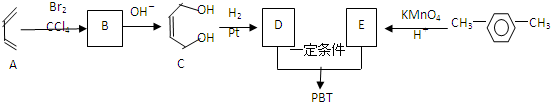
 互为同系物关系.
互为同系物关系.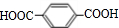 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$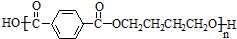 +(2n-1)H2O.
+(2n-1)H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
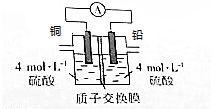 铅是一种活泼金属,铅与稀硫酸发生的反应为Pb+H2SO4(aq)═PbSO4(s)+H2↑,某同学根据反应设计如下装置:回答下列问题:
铅是一种活泼金属,铅与稀硫酸发生的反应为Pb+H2SO4(aq)═PbSO4(s)+H2↑,某同学根据反应设计如下装置:回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
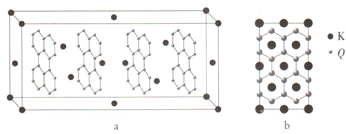 Q、R、X、Y、Z是原子序数依次增大的前四周期元素,Q的一种单质是天然存在的最硬的物质,X原子的核外电子有八种运动状态,Y元素的离子半径是第三周期中最小的,Z是第四周期中未成对电子最多的原子.
Q、R、X、Y、Z是原子序数依次增大的前四周期元素,Q的一种单质是天然存在的最硬的物质,X原子的核外电子有八种运动状态,Y元素的离子半径是第三周期中最小的,Z是第四周期中未成对电子最多的原子.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.35 mol/L | B. | 8.70 mol/L | C. | 10.05 mol/L | D. | 11.40 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | a | b | c |
| 合金质量/mg | 510 | 765 | 918 |
| 气体体积/mL | 560 | 672 | 672 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大于 57.3 kJ | B. | 等于 57.3 kJ | C. | 小于 57.3 kJ | D. | 无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com