
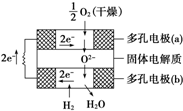
 2010年10月上海世博会临近结束的时刻,燃料电池车成为世博会上冉冉升起的新星.燃料电池是一种新型电池,它主要是利用燃料在氧化过程中把化学能直接转化为电能.氢氧燃料电池的突出优点是把化学能直接转变为电能,而不经过热能这一中间形式,它已用于宇宙飞船及潜艇中.
2010年10月上海世博会临近结束的时刻,燃料电池车成为世博会上冉冉升起的新星.燃料电池是一种新型电池,它主要是利用燃料在氧化过程中把化学能直接转化为电能.氢氧燃料电池的突出优点是把化学能直接转变为电能,而不经过热能这一中间形式,它已用于宇宙飞船及潜艇中.分析 (1)该燃料电池是将化学能转化为电能,负极上电极反应式为2H2+4OH--4e-=4H2O、正极反应式为O2+2H2O+4e-=4OH-,电池反应式为2H2+O2=2H2O,结合溶液中KOH是否浓度变化分析解答;
(2)根据电池反应式中水和转移电子的关系计算;
(3)该电池属于固体燃料电池,以固体氧化锆-氧化钇为电解质,电池工作时,正极上氧气得电子生成氧离子;负极为氢气失电子发生氧化反应生成水.
解答 解:(1)A.该电池中燃料不燃烧,是直接将化学能转化为电能,所以不能发出蓝色火焰,故A错误;
B.放电时反应过程中生成水,但反应保持在较高温度,使H2O蒸发,所以KOH浓度不变,则溶液的pH不变,故B错误;
C.通入氢气的电极为负极,通入氧气的电极为正极,故C错误;
D.负极上氢气失电子和氢氧根离子反应生成水,正极上氧气得电子生成氢氧根离子,所以负极:2H2+4OH--4e-=4H2O,正极:O2+2H2O+4e-=4OH-,故D正确;
故答案为:D;
(2)1L水的质量为1000g,水的物质的量为n=$\frac{m}{M}$=$\frac{1000g}{18g/mol}$=$\frac{500}{9}$mol,
负极:2H2-4e-+4OH-=4H2O ①
正极:O2+2H2O+4e-=4OH-②
①+②得:2H2+O2=2H2O~~~~转移电子
2mol 4mol
$\frac{500}{9}$mol 1.1×102 mol
故答案为:1.1×102 mol;
(3)该电池属于固体燃料电池,以固体氧化锆-氧化钇为电解质,电池工作时,正极上氧气得电子生成氧离子,则正极的反应式为O2+4e-═2O2-;负极为氢气失电子发生氧化反应生成水,则负极电极方程式为:2H2-4e-+2O2-═2H2O,正负极反应式相加可得总反应为:2H2+O2$\frac{\underline{\;高温\;}}{\;}$2H2O;
故答案为:O2+4e-═2O2-;2H2+O2$\frac{\underline{\;高温\;}}{\;}$2H2O.
点评 本题考查燃料电池,明确正负极上发生的反应以及电极方程式的书写方法是解本题关键,侧重于考查学生的分析能力和计算能力,注意把握电子守恒在计算中的应用,题目难度中等.


科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学卷(解析版) 题型:选择题
常温下,pH=11的氨水和pH=1的盐酸等体积混合后(不考虑溶液体积的变化),恰好完全反应。下列说法不正确的是
A.原氨水物质的量浓度为0.1mol·L-1
B.反应后的溶液中c(NH4+)+c (NH3·H2O)+c(NH3)=0.1mol·L-1
(NH3·H2O)+c(NH3)=0.1mol·L-1
C.反应后的溶液中:c(Cl-)>c(NH4+)>c(H+)>c( OH-)
D. 原氨水中:c(NH4+)+c(H+)=c(OH-)
原氨水中:c(NH4+)+c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
温度(K) CO2转化率(%) n(H2)/n(CO2) | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
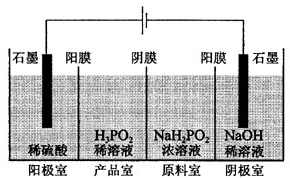 次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性.回答下列问题:
次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
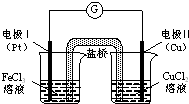
| A. | 电极Ⅰ上发生还原反应,作原电池的正极 | |
| B. | 电极Ⅱ的电极反应式为:Cu-2e-═Cu2+ | |
| C. | 该原电池的总反应为:2Fe3++Cu═Cu2++2Fe2+ | |
| D. | 盐桥中装有含氯化钾的琼脂,其作用是传递电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,5.2g乙炔和苯的混合气体中含有的碳原子数为0.4NA | |
| B. | 标准状况下,2.24L氖气所含原子数为0.2NA | |
| C. | 1mol硫酸氢钠固体中含阳离子总数2 NA | |
| D. | 5.6g Fe与足量的水蒸气完全反应,转移电子的数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
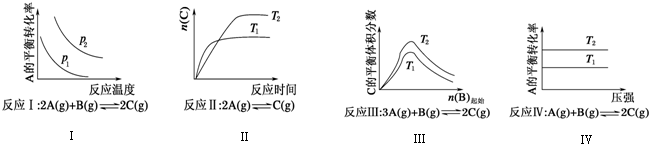
| A. | 反应Ⅰ:△H>0,p2>p1 | B. | 反应Ⅲ:△H>0,T2>T1或△H<0,T2<T1 | ||
| C. | 反应Ⅱ:△H>0,T1>T2 | D. | 反应Ⅳ:△H<0,T2>T1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com