
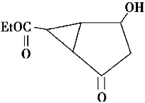
 及其核磁共振氢谱图如下:下列关于该有机物的叙述正确的是( )
及其核磁共振氢谱图如下:下列关于该有机物的叙述正确的是( )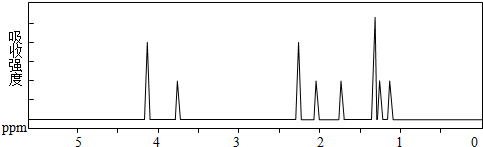
| A. | 该有机物不同化学环境的氢原子有6种 | |
| B. | 该有机物属于芳香族化合物 | |
| C. | 键线式中的Et代表的基团为-CH3 | |
| D. | 该有机物的分子式为C9H12O4 |
分析 A.该有机物结构不对称,含8种位置的H原子;
B.该有机物中不含苯环;
C.Et代表-CH2CH3;
D.由分子中原子个数确定分子式.
解答 解:A.该有机物结构不对称,核磁共振波谱图中有8种峰,含8种位置的H原子,故A错误;
B.该有机物中不含苯环,则不属于芳香族化合物,故B错误;
C.由结构及球棍模型可知,Et代表-CH2CH3,故C错误;
D.由1个分子中含9个C原子、12个H原子、4个O原子可知分子式为C9H12O4,故D正确;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,侧重于有机物知识的综合应用,注意把握有机物的结构特点和官能团的性质为解答该题的关键,题目难度不大.


科目:高中化学 来源:2016-2017学年山东省高一上10月月考化学试卷(解析版) 题型:选择题
下列关于氯气及含氯化合物的说法中,正确的是
A.液氯是氯气的水溶液,它能使干燥的有色布条褪色
B.氯气和NaOH溶液反应可制备消毒液
C.氯气可用于自来水的杀菌消毒,是因为氯气的毒性
D.新制饱和氯水在光照下有气泡产生,其主要成分是氯气
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原混合溶液中c(K+)为4mol/L | |
| B. | 原溶液中c(Cu2+)为1mol/L | |
| C. | 电解后溶液中c(H+)为8mol/L | |
| D. | 电解后加入1molCu(OH)2可使溶液复原 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a<b | B. | a>b | C. | a=b | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
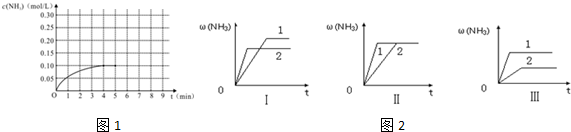
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
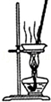 | 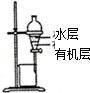 |
| A.装置可用于蒸干氯化铝溶液制AlCl3 | B.装置可用于分离CCl4萃取碘水后已分层的有机层和水层 |
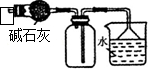 | 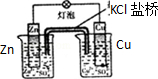 |
| C.装置可用于收集NH3或HCl气体,并防止倒吸 | D.装置盐桥中的K+自右向左移动 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑥ | B. | ①③⑥ | C. | ③⑤⑥⑦ | D. | ②③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡向正反应方向移动了 | B. | 物质A的转化率减少了 | ||
| C. | 物质B的质量增重了 | D. | a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
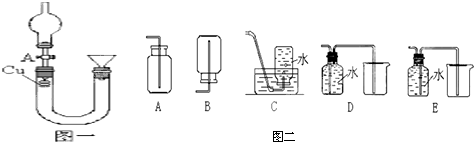

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com