

| A.锌极附近滴入酚酞,溶液呈红色。 |
| B.铁极发生的电极反应为:2H2O+O2+4e=4OH- |
| C.铁极发生吸氧腐蚀生成锈蚀 |
| D.溶液中的OH-离子向铁极移动 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.锌做负极 | B.放电时,正极产物是银 |
| C.电解质溶液不可能呈酸性 | D.充电时发生了原电池反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
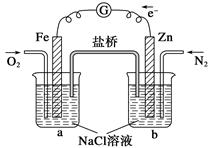
| A.烧杯a中的溶液pH降低 |
| B.烧杯b中发生氧化反应 |
| C.烧杯a中发生的反应为2H++2e-===H2 |
| D.烧杯b中发生的反应为2Cl--2e-===Cl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.电子通过外电路从b极流向a极 |
| B.b极上的电极反应式为:O2+2H2O+4e-=4OH- |
| C.每转移0.1 mol电子,消耗1.12 L的H2 |
| D.H+由a极通过固体酸电解质传递到b极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电池内部H+由正极向负极移动 |
| B.另一极的电极反应式为:O2+4e—+2H2O=4OH— |
| C.乙醇在正极发生反应,电子经过外电路流向负极 |
| D.电池总反应为:2CH3CH2OH + O2→2CH3CHO + 2H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
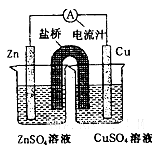
| A.一段时间后两烧杯中c(Zn2+)、c(Cu2+)均减小 |
| B.原电池工作时,Cu电极流出电子,发生氧化反应 |
| C.原电池工作时的总反应为Zn+Cu2+=Zn2++Cu |
| D.盐桥中装有含氯化钾的琼脂,其作用是传递电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.手机上用的锂离子电池属于二次电池 |
| B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 |
| C.甲醇燃料电池可把化学能转化为电能 |
| D.锌锰干电池中,锌电极是负极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2H2O设计成原电池。
2H2O设计成原电池。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com