
| A. | 0.9 g H2O中含有电子数为NA | |
| B. | 11.2 LCl2中含有的原子数为NA | |
| C. | 4℃、101.3kPa时,54mL H2O中含有的分子数为3NA | |
| D. | 2L 1mol/L Na2SO4溶液中离子总数为3NA |
分析 A、求出水的物质的量,然后根据水为10电子微粒来分析;
B、氯气所处的状态不明确;
C、4℃、101.3kPa时,水的密度为1g/mL;
D、Na2SO4溶液中除了钠离子、硫酸根还有氢离子和氢氧根.
解答 解:A、0.9g水的物质的量为n=$\frac{0.9g}{18g/mol}$=0.05mol,而水为10电子微粒,故0.05mol水中含0.5mol电子即0.5NA个,故A错误;
B、氯气所处的状态不明确,故无法计算氯气的物质的量和含有的原子个数,故B错误;
C、4℃、101.3kPa时,水的密度为1g/mL,故54mL水的质量为54g,则其分子个数N=$\frac{54g}{18g/mol}×{N}_{A}/mol$=3NA个,故C正确;
D、Na2SO4溶液中除了钠离子、硫酸根还有氢离子和氢氧根,故溶液中的离子总数大于3NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
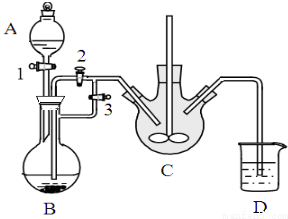 乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,M=288g/mol)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:CH3CH(OH)COOH+FeCO3+2H2O→[CH3CH(OH)COO]2Fe•3H2O+CO2↑.
乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,M=288g/mol)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:CH3CH(OH)COOH+FeCO3+2H2O→[CH3CH(OH)COO]2Fe•3H2O+CO2↑.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.75mol | B. | 1.25mol | C. | 1.5mol | D. | 2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 符合通式CnH2nO3 | B. | 和乙醇中化学键类型相同 | ||
| C. | 能和金属钠反应 | D. | 能使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在0.1 mol•L-1NaHCO3溶液中:c(Na+)>c(OH-)>c(HCO3-)>c(H+)>c(CO32-) | |
| B. | 在0.1 mol•L-1Na2CO3溶液中:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) | |
| C. | 一定量(NH4)2SO4与NH3•H2O混合所得的酸性溶液中:c(NH4+)<2c(SO42-) | |
| D. | 向0.4 mol/L CH3COOK溶液中加入等体积1.2 mol/L HCl溶液:c(CH3COO-)+c(CH3COOH)=0.4 mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com