
【题目】喷气式飞机在对流层中飞行时排放的尾气NO,能进行下列反应:O3→O2+O;NO+O3→NO2+O2,NO2+O→NO+O2,则NO在这些反应中的作用是( )
A.催化剂B.还原剂C.氧化剂D.中间产物
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】从精炼钢的阳极泥中(主要成分为Cu2Te)回收碲的工艺流程如下:

请回答下列问题:
(1)“焙烧”后,碲主要以TeO2形式存在,则每生成32gTeO2,反应转移电子的物质的量为____________mol。
(2)为选择最佳焙烧工艺,进行温度和硫酸加入量的条件试验,结果如下表所示:

则实验中应选择的条件为________________________。
(3)“氧化”时的溶液温度不宜过高,原因为________________________。
(4)工艺(I)中,“还原”时发生的总离子方程式为______________________________。H2SO4和Na2SO3可用浓盐酸代替,但缺点为______________________________________。
(5)工艺(II)中,“浸出液电积”时产生碲粉的电极反应式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某温度时,在一个10L恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:

(1)该反应的化学方程式为_________________。
(2)反应开始至2min,以气体X表示的平均反应速率为________________。
(3)平衡时容器内气体的压强与起始时比________________(填“变大”,“变小”或“相等”下同),混合气体的密度与起始时比________________。
(4)将amolX与bmolY的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=2n(Z),则原混合气体中a:b=____。
Ⅱ.在恒温恒压的密闭容器中,当下列物理量不再发生交化时:①混合气体的压强;②混合气体的密度;③混合气体的总物质的量;④混合气体的平均相对分子质量;⑤各反应物或生成物的反应速率之比等于化学计量数之比
(1)一定能证明2NO2(g)![]() N2O4(g)达到平衡状态的是________(填序号,下同)。
N2O4(g)达到平衡状态的是________(填序号,下同)。
(2)一定能证明NH2COONH4(s)![]() CO2(g)+2NH3(g)达到平衡状态的是______。
CO2(g)+2NH3(g)达到平衡状态的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的的是( )
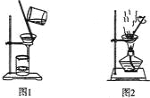
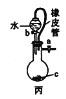
① 用图1所示装置从Fe(OH)3胶体中过滤出Fe(OH)3胶粒
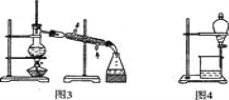
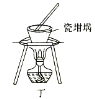
② 用图2所示装置蒸发掉CuCl2溶液中部分水制得CuCl2·2H20晶体
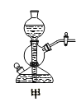
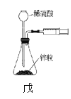
③用图3所示装置从CH3OH与C4H9OH的混合物中分离出甲醇
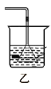
④用图4所示装置从C2H5OH与C2H5OOCCH3的混合物中分离出乙酸乙酯
⑤用甲装置实验室制取乙炔 ⑥乙装置下层CCl4、上层水漏斗在CCl4层,吸收HCl气体
⑦用丙装置测量气体可以减少误差 ⑧用丁装置加热融化NaOH固体
⑨用戊装置测量产生气体的体积
A. ①③⑤⑥ B. ③⑥⑦ C. ③⑥⑦⑧ D. ②④⑦⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2O2是一种常见的过氧化物,具有强氧化性和漂白性。 通常可用作漂白剂和呼吸面具中的供氧剂。
(1)某实验小组通过下列实验探究过氧化钠与水的反应:

①用化学方程式解释使酚酞试液变红的原因___________________,依据实验现象推测红色褪去的原因是________________。
②加入MnO2的作用为_______________________。
(2)某实验小组拟验证CO2与Na2O2反应的产物,现设计以下实验装置进行实验:


①写出装置A中反应的化学方程式____________________;
②拟用装置D收集气体产物,请在方框中将装置补充完整______。
③产物检验:检验气体产物的方法:___________________;
④有同学认为该实验装置存在明显缺陷,你认为该缺陷是什么____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)![]() 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:

① b<f ② 915℃、2.0 MPa时E的转化率为60% ③ 增大压强平衡左移 ④ K(1 000℃)>K(810℃) 上述①~④中正确的有( )
A. 4个 B. 3个 C. 2个 D. 1个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式书写正确的是
A.碳酸的电离方程式:H2CO3 ![]() 2H+ + CO32-
2H+ + CO32-
B. 硫化钠水解: S2-+2H2O![]() H2S +2OH-
H2S +2OH-
C.往AgI悬浊液中滴加Na2S饱和溶液:2Ag+ (aq)+ S2-(aq) = Ag2S(s)
D.用醋酸除水垢: 2CH3COOH + CaCO3 = 2CH3COO- + Ca2+ + H2O + CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X、Q、Y、Z、M、R均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3:4,M原子的最外层电子数与次外层电子数之比为3:4;R-、Z+、X+离子半径逐渐减小;化合物XR常温下为气体,Q和Y在周期表中的位置相邻,请回答下列问题:
(1)写出单质R的一种工业用途_______________________。
(2)M和R的最高价氧化物的水化物中酸性最强的是___________(用化学式表示)。
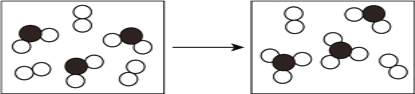
(3)下图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,写出该转化过程的化学方程式为____________________。
(4)由X、Y、Z、M四种元素组成的一种离子化合物A,已知A,既能与盐酸反应,又能与氢氧化钠溶液反应,还能和氯水反应,写出A与氯水反应的离子方程式___________。
(5)科学家认为存在QX5这种物质,且预测其与水剧烈反应放出气体,所得水溶液呈弱碱性,已知QX5中含有离子键和极性键,写出化合物的电子式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是重要的化工原料,以乙烯为原料在不同条件下可合成下列物质(部分条件未标出):

按下列要求写出:
(1)聚乙烯的结构简式是_____________,乙醛的结构简式是_____________;
(2)反应①的化学方程式是________________________________,反应类型是___________;
(3)反应③的化学方程式是________________________________,反应类型是___________;
(4)反应⑤的化学方程式是________________________________,反应类型是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com