
ij¶žŌŖĖį(H2A)°“ĻĀŹ½·¢ÉśµēĄė£ŗH2A=H£«£«HA££»HA£ H£«£«A2£”£ĻÖÓŠĻĀĮŠĖÄÖÖČÜŅŗ£ŗ
H£«£«A2£”£ĻÖÓŠĻĀĮŠĖÄÖÖČÜŅŗ£ŗ
¢Ł0.01 mol”¤L£1µÄH2AČÜŅŗ
¢Ś0.01 mol”¤L£1µÄNaHAČÜŅŗ
¢Ū0.02 mol”¤L£1µÄHClČÜŅŗÓė0.04 mol”¤L£1µÄNaHAČÜŅŗµČĢå»ż»ģŗĻ
¢Ü0.02 mol”¤L£1µÄNaOHČÜŅŗÓė0.02 mol”¤L£1µÄNaHAČÜŅŗµČĢå»ż»ģŗĻ
ĻĀĮŠ¹ŲÓŚÉĻŹöĖÄÖÖČÜŅŗµÄĖµ·Ø²»ÕżČ·µÄŹĒ (””””)
A£®ČÜŅŗ¢ŚÖŠ“ęŌŚĖ®½āĘ½ŗā£ŗHA££«H2O H2A£«OH£
H2A£«OH£
B£®ČÜŅŗ¢ŪÖŠÓŠ£ŗc(HA£)£«c(A2£)£½c(Na£«)
C£®ČÜŅŗ¢ÜÖŠÓŠ£ŗc(OH£)£½c(H£«)£«c(HA£)
D£®ĖÄÖÖČÜŅŗÖŠc(HA£)“󊔣ŗ¢Ū>¢Ł>¢Ś>¢Ü
 ČżŠĀæģ³µ½šÅĘÖÜÖÜĮ·ĻµĮŠ“š°ø
ČżŠĀæģ³µ½šÅĘÖÜÖÜĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
Ä³ŃŠ¾æŠŌѧĻ°Š”×éĪŖĮĖĢ½¾æ“×ĖįµÄµēĄėĒéæö£¬½ųŠŠĮĖČēĻĀŹµŃ锣
ŹµŃéŅ»£ŗÅäÖĘ²¢±ź¶Ø“×ĖįČÜŅŗµÄÅضČ
Č”±ł“×ĖįÅäÖĘ250 mL 0.2 mol/LµÄ“×ĖįČÜŅŗ£¬ÓĆ0.2 mol/LµÄ“×ĖįČÜŅŗĻ”ŹĶ³ÉĖłŠčÅØ¶ČµÄČÜŅŗ£¬ŌŁÓĆNaOH±ź×¼ČÜŅŗ¶ŌĻ”ŹĶŗó“×ĖįČÜŅŗµÄÅØ¶Č½ųŠŠ±ź¶Ø”£»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)ÅäÖĘ250 mL 0.2 mol/L“×ĖįČÜŅŗŹ±ŠčŅŖÓƵ½µÄ²£Į§ŅĒĘ÷ÓŠĮæĶ²”¢ÉÕ±”¢²£Į§°ō”¢________ŗĶ________”£
(2)ĪŖ±ź¶Øij“×ĖįČÜŅŗµÄ×¼Č·ÅØ¶Č£¬ÓĆ0.2000 mol/LµÄNaOHČÜŅŗ¶Ō20.00 mL“×ĖįČÜŅŗ½ųŠŠµĪ¶Ø£¬¼ø“ĪµĪ¶ØĻūŗÄNaOHČÜŅŗµÄĢå»żČēĻĀ£ŗ
| ŹµŃéŠņŗÅ | 1 | 2 | 3 | 4 |
| ĻūŗÄNaOHČÜŅŗµÄĢå»ż(mL) | 20.05 | 20.00 | 18.50 | 19.95 |
| “×ĖįÅضČ(mol/L) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
Ė®µÄµēĄėĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾:
ČōŅŌAµć±ķŹ¾25 ”ꏱĖ®µēĄėĘ½ŗāŹ±µÄĄė×ÓµÄÅضČ,µ±ĪĀ¶ČÉżøßµ½100 ”ꏱ,Ė®µÄµēĄėĘ½ŗāדĢ¬µ½Bµć,Ōņ“ĖŹ±Ė®µÄĄė×Ó»ż“Ó””””””Ōö¼Óµ½””””””,Ōģ³ÉĖ®µÄĄė×Ó»żŌö“óµÄŌŅņŹĒ”””””””””””””””””””””””””””””£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ŌŚŅ»¶ØĪĀ¶ČĻĀ,±ł“×Ėį¼ÓĖ®Ļ”ŹĶ¹ż³ĢÖŠ,ČÜŅŗµÄµ¼µēÄÜĮ¦ČēĻĀĶ¼ĖłŹ¾,Ēė»Ų“š:
(1)”°O”±µćµ¼µēÄÜĮ¦ĪŖ0µÄĄķÓÉŹĒ”””””””””””””””””£
(2)A”¢B”¢CČżµćČÜŅŗc(H+)ÓÉŠ”µ½“óµÄĖ³ŠņĪŖ”””””””””””””””””””””””””””””””””””””£
(3)ČōŹ¹CµćČÜŅŗÖŠc(CH3COO-)Ōö“óµÄĶ¬Ź±ČÜŅŗµÄc(H+)¼õŠ”,æɲÉČ”µÄ“ėŹ©ŹĒ:
¢Ł””””””””””;¢Ś””””””””””;¢Ū”””””””””””£
(4)¾ŹµŃé²āµĆCµć“¦:c(CH3COOH)="0.1" mol”¤L-1,c(CH3COO-)="0.01" mol”¤L-1,ŌņøĆĢõ¼žĻĀCH3COOHµÄµēĄė³£ŹżKa=”””””””””£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ĻÖÓŠÅØ¶Č¾łĪŖ0.1 mol/LµÄĻĀĮŠČÜŅŗ£ŗ
¢ŁĮņĖį””¢Ś“×Ėį””¢ŪĒāŃõ»ÆÄĘ””¢ÜĀČ»Æļ§
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)¢Ł¢Ś¢Ū¢ÜĖÄÖÖČÜŅŗÖŠÓÉĖ®µēĄė³öµÄH£«ÅضČÓɓ󵽊”µÄĖ³ŠņŹĒ(ĢīŠņŗÅ)________”£
(2)½«¢ŪŗĶ¢ÜµČĢå»ż»ģŗĻŗ󣬻ģŗĻŅŗÖŠø÷Ąė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņŹĒ____”£
(3)ŅŃÖŖT ”ę£¬KW£½1”Į10£13£¬Ōņt ”ę________(Ģī”°>”±”¢”°<”±»ņ”°£½”±)25”ę”£ŌŚT”ꏱ½«pH£½11µÄNaOHČÜŅŗa LÓėpH£½1µÄH2SO4ČÜŅŗb L»ģŗĻ(ŗöĀŌ»ģŗĻŗóČÜŅŗĢå»żµÄ±ä»Æ)£¬ČōĖłµĆ»ģŗĻČÜŅŗµÄpH£½10£¬Ōņa”Ćb£½________”£
(4)25”ꏱ£¬ÓŠpH£½xµÄŃĪĖįŗĶpH£½yµÄĒāŃõ»ÆÄĘČÜŅŗ(x”Ü6£¬y”Ż8)£¬Č”a LøĆŃĪĖįÓėb LøĆĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦£¬Ē”ŗĆĶźČ«ÖŠŗĶ£¬Ēó£ŗ
¢ŁČōx£«y£½14£¬Ōņa/b£½________(ĢīŹż¾Ż)£»
¢ŚČōx£«y£½13£¬Ōņa/b£½________(ĢīŹż¾Ż)£»
¢ŪČōx£«y>14£¬Ōņa/b£½________(Ģī±ķ“ļŹ½)£»
¢ÜøĆŃĪĖįÓėøĆĒāŃõ»ÆÄĘČÜŅŗĶźČ«ÖŠŗĶ£¬Į½ČÜŅŗµÄpH(x”¢y)µÄ¹ŲĻµŹ½ĪŖ__(Ģī±ķ“ļŹ½)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
(““ŠĀŌ¤²āĢā)ŅŃÖŖ25 ”ꏱČõµē½āÖŹµÄµēĄėĘ½ŗā³£Źż£ŗ
Ka(CH3COOH)£½1.8”Į10£5£¬Ka(HSCN)£½0.13”£
(1)½«20 mL 0.10 mol”¤L£1 CH3COOHČÜŅŗŗĶ20 mL 0.10 mol”¤L£1µÄHSCNČÜŅŗ·Ö±šÓė0.10 mol”¤L£1µÄNaHCO3ČÜŅŗ·“Ó¦£¬ŹµŃé²āµĆ²śÉśCO2ĘųĢåĢå»ż(V)Óė
Ź±¼ätµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£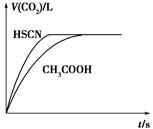
·“Ó¦æŖŹ¼Ź±£¬Į½ÖÖČÜŅŗ²śÉśCO2µÄĖŁĀŹĆ÷ĻŌ²»Ķ¬µÄŌŅņŹĒ________£»·“Ó¦½įŹųŗóĖłµĆČÜŅŗÖŠc(SCN£)______c(CH3COO£)(Ģī”°£¾”±”¢”°£½”±»ņ£¼)”£
(2)2.0”Į10£3 mol”¤L£1µÄĒā·śĖįĖ®ČÜŅŗÖŠ£¬µ÷½ŚČÜŅŗpH(ŗöĀŌµ÷½ŚŹ±Ģå»ż±ä»Æ)£¬²āµĆĘ½ŗāĢåĻµÖŠc(F£)”¢c(HF)ÓėČÜŅŗpHµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£Ōņ25 ”ꏱ£¬HFµēĄėĘ½ŗā³£ŹżĪŖKa(HF)£½________(ĮŠŹ½ĒóÖµ)”£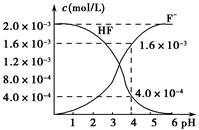
(3)ÄŃČÜĪļÖŹCaF2ČܶȻż³£ŹżĪŖKsp£½1.5”Į10£10£¬½«4.0”Į10£3 mol”¤L£1 HFČÜŅŗÓė4.0”Į10£4 mol”¤L£1µÄCaCl2ČÜŅŗµČĢå»ż»ģŗĻ£¬µ÷½ŚČÜŅŗpH£½4(ŗöĀŌµ÷½ŚŹ±ČÜŅŗĢå»ż±ä»Æ)£¬ŹŌ·ÖĪö»ģŗĻŗóŹĒ·ńÓŠ³ĮµķÉś³É£æ________(Ģī”°ÓŠ”±»ņ”°Ć»ÓŠ”±)£¬¼ņŹöĄķÓÉ£ŗ_____________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ļ®±»ÓžĪŖ”°½šŹōĪ¶¾«”±£¬ŅŌLiCoO2ĪŖÕż¼«²ÄĮĻµÄļ®Ąė×Óµē³ŲŅѱ»¹ć·ŗÓĆ×÷±ćŠÆŹ½µēŌ“”£¹¤ŅµÉĻ³£ŅŌ¦Ā-ļ®»Ōæó(Ö÷ŅŖ³É·ÖĪŖLiAlSi2O6£¬»¹ŗ¬ÓŠFeO”¢MgO”¢CaOµČŌÓÖŹ)ĪŖŌĮĻĄ“ÖĘČ”½šŹōļ®”£ĘäÖŠŅ»ÖÖ¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ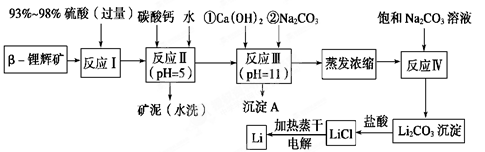
ŅŃÖŖ£ŗ¢Ł²æ·Ö½šŹōĒāŃõ»ÆĪļæŖŹ¼³ĮµķŗĶĶźČ«³ĮµķŹ±µÄpH£ŗ
| ĒāŃõ»ÆĪļ | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| æŖŹ¼³ĮµķpH | 2£®7 | 3.7 | 9.6 |
| ĶźČ«³ĮµķpH | 3.7 | 4.7 | 11 |
| ĪĀ¶Č/”ę | 0 | 10 | 20 | 50 | 75 | 100 |
| Li2CO3µÄČܽā¶Č/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ĻÖÓŠÅØ¶Č¾łĪŖ0£®1mol µÄĻĀĮŠČÜŅŗ£ŗ¢ŁĮņĖį”¢¢Ś“×Ėį”¢¢ŪĒāŃõ»ÆÄĘ”¢¢ÜĀČ»Æļ§”¢¢Ż“×Ėįļ§”¢¢ŽĮņĖįĒāļ§”¢¢ß°±Ė®£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
µÄĻĀĮŠČÜŅŗ£ŗ¢ŁĮņĖį”¢¢Ś“×Ėį”¢¢ŪĒāŃõ»ÆÄĘ”¢¢ÜĀČ»Æļ§”¢¢Ż“×Ėįļ§”¢¢ŽĮņĖįĒāļ§”¢¢ß°±Ė®£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(l)¢Ł”¢¢Ś”¢¢Ū”¢¢ÜĖÄÖÖČÜŅŗÖŠÓÉĖ®µēĄė³öµÄÅضČÓɓ󵽊”µÄĖ³ŠņŹĒ___________________
_____________________________________£ØĢīŠņŗÅ£©”£
£Ø2£©¢Ü”¢¢Ż”¢¢Ž”¢¢ßĖÄÖÖČÜŅŗÖŠNH4+ÅضČÓɓ󵽊”µÄĖ³ŠņŹĒ_________________£ØĢīŠņŗÅ£©”£
£Ø3£©½«¢ŪŗĶ¢Ü°“Ģå»ż±Čl£ŗ2»ģŗĻŗó£¬ČÜŅŗµÄpH>7£¬Ōņ»ģŗĻŅŗÖŠø÷Ąė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņŹĒ________________________________________”£
£Ø4£©ŅŃÖŖt”ꏱ£¬Kw=1”Į10 £¬Ōņt”ę__________£ØĢī”°>”±”¢”°<”±»ņ”°=”±£©25”ę”£ŌŚt”ꏱ½«pH=11µÄNaOHČÜŅŗaLÓėpH=1µÄH2SO4ČÜŅŗbL»ģŗĻ£ØŗöĀŌ»ģŗĻŗóČÜŅŗĢå»żµÄ±ä»Æ£©£¬ČōĖłµĆ»ģŗĻČÜŅŗµÄpH=2£¬Ōņ a:b=______________”£
£¬Ōņt”ę__________£ØĢī”°>”±”¢”°<”±»ņ”°=”±£©25”ę”£ŌŚt”ꏱ½«pH=11µÄNaOHČÜŅŗaLÓėpH=1µÄH2SO4ČÜŅŗbL»ģŗĻ£ØŗöĀŌ»ģŗĻŗóČÜŅŗĢå»żµÄ±ä»Æ£©£¬ČōĖłµĆ»ģŗĻČÜŅŗµÄpH=2£¬Ōņ a:b=______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ŅŃÖŖ25 ”ꏱ²æ·ÖČõµē½āÖŹµÄµēĄėĘ½ŗā³£ŹżŹż¾ŻČēĻĀ±ķ:
| »ÆѧŹ½ | CH3COOH | H2CO3 | HClO | |
| Ę½ŗā ³£Źż | Ka=1.8”Į10-5 | 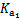 = =4.3”Į10-7 | 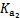 = =5.6”Į10-11 | Ka= 3.0”Į10-8 |
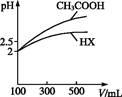
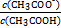 =”””””””””””£
=”””””””””””£ ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com