
| A. | 元素的金属性:B>A;元素的非金属性:D>C | |
| B. | 原子序数:b>a>c>d | |
| C. | 离子半径:D2->C->B2+>A+ | |
| D. | 原子半径:A>B>C>D |
分析 aA+、bB2+、cC-、dD2-四种离子均具有相同的电子层结构,则有:a-1=b-2=c+1=d+2,可知原子序数:b>a>c>d,由离子所带电荷可知,C、D为非金属,应处于第二周期,故C为F元素,D为O元素,A、B为金属,应处于第三周期,A为Na元素,B为Mg元素,结合元素周期律解答.
解答 解:aA+、bB2+、cC-、dD2-四种离子均具有相同的电子层结构,则有:a-1=b-2=c+1=d+2,可知原子序数:b>a>c>d,由离子所带电荷可知,C、D为非金属,应处于第二周期,故C为F元素,D为O元素,A、B为金属,应处于第三周期,A为Na元素,B为Mg元素.
A.同周期随原子序数增大,金属性减弱、非金属性增强,故元素的金属性:Mg<Na,元素的非金属性:O>F,故A错误;
B.四种离子均具有相同的电子层结构,则有:a-1=b-2=c+1=d+2,可知原子序数:b>a>c>d,故B正确;
C.原子序数:b>a>c>d,电子层结构相同,核电荷数越大离子半径越小,则离子半径:D2->C->A+>B2+,故C错误;
D.同周期元素从左到右原子半径逐渐减小,、同主族自上而下原子半径增大,故则原子半径大小为:A>B>D>C,故D错误,
故选B.
点评 本题考查结构与位置关系、元素周期律等,难度中等,注意元素周期律的理解掌握,也可以根据电荷与核外电子排布相同推断元素在周期表中的位置而不需要推断具体的元素.


科目:高中化学 来源: 题型:选择题
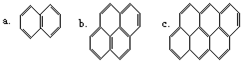 在沥青的蒸气中含有稠环芳香烃,其中一些成分可视为“同系物”,如:以此顺序推测还可以有d、e、f…等,在该系列化合物中,碳的最大百分含量是( )
在沥青的蒸气中含有稠环芳香烃,其中一些成分可视为“同系物”,如:以此顺序推测还可以有d、e、f…等,在该系列化合物中,碳的最大百分含量是( )| A. | 100% | B. | 56% | C. | 97.3% | D. | 93.8% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 目前发现的所有元素占据了周期表里全部位置,不可能再有新的元素被发现 | |
| B. | 元素的性质随着原子序数的增加而呈周期性变化 | |
| C. | 俄国化学家道尔顿为元素周期表的建立作出了巨大贡献 | |
| D. | 目前已知发现的第ⅥA族元素为5种,所以该族元素共有5种单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在水中能电离出离子的化合物一定是离子化合物 | |
| B. | CO2分子中含极性键,且溶于水能导电,所以CO2是电解质 | |
| C. | Ca(OH)2微溶于水,所以是弱电解质 | |
| D. | CH3COOH在水中只能部分电离,所以是弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
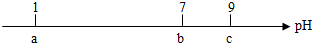
| A. | 常温下,0.1mol•L-1的HCl溶液的pH=1 | |
| B. | 当pH=7时,所加NH3•H2O溶液的体积大于10mL | |
| C. | 当7<pH<9时,溶液中c(NH4+)>c(Cl-) | |
| D. | 继续滴加0.1mol•L-1的NH3•H2O溶液,溶液的pH最终可以变化至13 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13C和14C属于同一种元素,它们互为同位素 | |
| B. | 1H和2H是不同的核素,它们的质子数相同 | |
| C. | 14C和14N的质量数相同,它们的中子数不等 | |
| D. | 6Li和7Li电子数相同,中子数也相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 给容器消毒 | B. | 杀死果实周围的细菌,防止霉变 | ||
| C. | 延长果实或花朵的寿命 | D. | 催熟果实或花朵 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com