
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH 变化曲线如图所示。下列判断正确的是( )
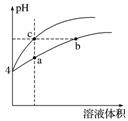
A.a、c两点溶液的导电能力相同
B.a、b、c三点溶液水的电离程度a>b>c
C.b点溶液中c(H+)+c(NH3·H2O)=c(OH-)
D.用等浓度NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液体积Vb=Vc
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
已知Al2O3(s)+AlCl3(g)+3C(s)===3AlCl(g)+3CO(g) ΔH=a kJ·mol-1
判断下列变化过程是否正确,正确的划“√”,错误的划“×”
(1)3AlCl(g)+3CO(g)===Al2O3(s)+AlCl3(g)+3C(s)
ΔH=a kJ·mol-1( )
(2)AlCl(g)+CO(g)===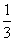 Al2O3(s)+
Al2O3(s)+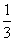 AlCl3(g)+3C(s)
AlCl3(g)+3C(s)
ΔH=-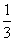 a kJ·mol-1( )
a kJ·mol-1( )
(3)2Al2O3(s)+2AlCl3(g)+6C(s)===6AlCl(g)+6CO(g)
ΔH=-2a kJ·mol-1( )
查看答案和解析>>
科目:高中化学 来源: 题型:
374 ℃、22.1 MPa以上的超临界水具有很强的溶解有机物的能力,并含有较多的H+和OH-,由此可知超临界水 ( )
A.显中性,pH等于7
B.表现出非极性溶剂的特性
C.显酸性,pH小于7
D.表现出极性溶剂的特性
查看答案和解析>>
科目:高中化学 来源: 题型:
现有两瓶温度分别为15 ℃和45 ℃,pH均为1的硫酸溶液,下列有关说法不正确的是( )
A.两溶液中的c(OH-)相等
B.两溶液中的c(H+)相同
C.等体积两种溶液中和碱的能力相同
D.两溶液中的c(H2SO4)基本相同
查看答案和解析>>
科目:高中化学 来源: 题型:
重铬酸铵[(NH4)2Cr2O7]是一种橘黄色晶体,可用作有机合成催化剂、实验室制纯净的N2及Cr2O3等。实验室可由工业级铬酸钠(Na2CrO4)制取重铬酸铵。有关物质的溶解度如图所示。

实验步骤如下:
步骤1:将铬酸钠溶于适量的水,加入一定量浓硫酸酸化,使铬酸钠转化为重铬酸钠。
步骤2:将上述溶液蒸发结晶,并趁热过滤。
步骤3:将步骤2得到的晶体再溶解,再蒸发结晶并趁热过滤。
步骤4:将步骤2、3得到的滤液冷却至40 ℃左右进行结晶,用水洗涤,获得重铬酸钠晶体。
步骤5:将步骤4得到的重铬酸钠和氯化铵按物质的量之比1∶2 溶于适量的水中,加热至105~110 ℃,让其充分反应。
(1)步骤1是一个可逆反应,该反应的离子方程式为_____________。
(2)步骤2、3的主要目的是_______________________________________。
(3)步骤4在40 ℃左右结晶,其主要目的是________________________________。
(4)步骤5获得(NH4)2Cr2O7还需补充的操作有_________________________________。
(5)(NH4)2Cr2O7受热分解制取Cr2O3的化学方程式为_____________________________。
(6)对上述产品进行检验和含量测定。
①检验产品中是否含有K+的实验方法是_________________________________。
②为了测定上述产品中(NH4)2Cr2O7的含量,称取样品0.150 0 g,置于锥形瓶中,加50 mL水,再加入2 g KI(过量)及稍过量的稀硫酸溶液,摇匀,暗处放置10 min,然后加150 mL蒸馏水并加入3 mL 0.5%淀粉溶液,用0.100 0 mol·L-1 Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液30.00 mL,则上述产品中(NH4)2Cr2O7的纯度为__________(假定杂质不参加反应,已知:Cr2O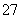 +6I-+14H+===2Cr3++3I2+7H2O,I2+2S2O
+6I-+14H+===2Cr3++3I2+7H2O,I2+2S2O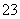 ===2I-+S4O
===2I-+S4O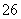 )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
第四周期中,未成对电子数最多的元素是__________。(填名称)
(1)它位于第________族。
(2)核外电子排布式是________。
(3)它有________个能层,________个能级,__________种运动状态不同的电子。
(4)价电子排布式________,价电子排布图__________。
(5)属于________区。
查看答案和解析>>
科目:高中化学 来源: 题型:
前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子数相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。
四种元素中的第一电离能最小的是__________,电负性最大的是__________。(填元素符号)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com