
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源:不详 题型:单选题
| A.HCOOH、H2CO3、H2SO4分子中均含有两个氢原子,都是二元酸 |
| B.H2O、HCOOH、Cu2(OH)2CO3均含有氧元素,都是氧化物 |
| C.HF、CH3COOH、CH3CH2OH都易溶于水,都是电解质 |
| D.HClO、HNO3、浓H2SO4都具强氧化性,都是氧化性酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.I-→I2 | B.Na2SO3→SO2 |
| C.SO2→S | D.HCO3-→CO32- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
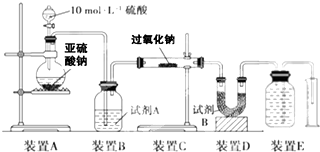
查看答案和解析>>
科目:高中化学 来源:松江区模拟 题型:问答题
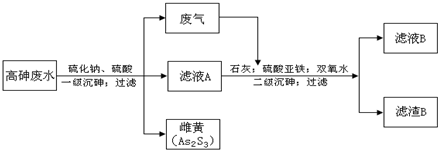
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只有①正确 | B.只有③ | C.只有①和④ | D.①②③④都正确 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铁粉放入硫酸铜溶液 |
| B.CO2气体通入澄清石灰水 |
| C.大理石高温分解 |
| D.KClO3在MnO2催化下加热制O2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2S+2HNO3═S↓+2NO2↑+2H2O |
| B.CuO+2HNO3═Cu(NO3)2+H2O |
| C.4HNO3═4NO2↑+O2↑+2H2O |
| D.3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com