
分析 (1)m(NH3)=n(NH3).M(NH3)=$\frac{672L}{22.4L/mol}$×17g/mol=510g,溶剂的质量为1000g,溶液质量分数=$\frac{溶质的质量}{溶质的质量+溶剂的质量}×100%$;
(2)n(NH3)=$\frac{672L}{22.4L/mol}$=30mol,溶液体积=$\frac{510g+1000g}{0.755g/mL}$=2L,则氨水物质的量浓度=$\frac{n}{V}$.
解答 解:(1)m(NH3)=n(NH3).M(NH3)=$\frac{672L}{22.4L/mol}$×17g/mol=510g,溶剂的质量为1000g,溶液质量分数=$\frac{溶质的质量}{溶质的质量+溶剂的质量}×100%$=$\frac{510g}{510g+1000g}$×100%=33.8%,
故答案为:33.8%;
(2)n(NH3)=$\frac{672L}{22.4L/mol}$=30mol,溶液体积=$\frac{510g+1000g}{0.755g/mL}$=2L,则氨水物质的浓度=$\frac{30mol}{2L}$=15mol/L,
故答案为:15mol/L.
点评 本题考查物质的量浓度计算,为高频考点,侧重考查学生分析判断及计算能力,明确各个物理量之间的关系式是解本题关键,注意:溶液体积不等于氨气体积与水体积之和,为易错点.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
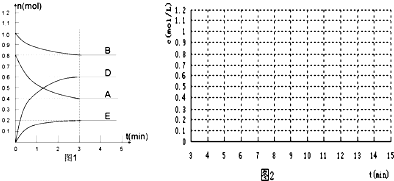
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下pH=7的溶液中:Fe3+、Mg2+、SO42-、Cl-能大量共存 | |
| B. | 在含有0.1mol•L-1 Fe3+的溶液中:SCN-、Cl-、K+不能大量共存 | |
| C. | 在含有HCO3-、SO32-、S2-、CH3COO-四种阴离子的溶液中加入足量的Na2O2固体后,CH3COO-浓度变化最小 | |
| D. | 常温下,水电离出c(H+)=10-10的溶液中:Na+、ClO-、S2-、NH4+不能大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol H2含有的分子数目为NA | |
| B. | 24g Mg变为Mg2+时失去的电子数目为NA | |
| C. | 1L 1mol•L-1CaCl2溶液中含有的Cl-离子数目为NA | |
| D. | 常温常压下,11.2LO2中含有的原子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
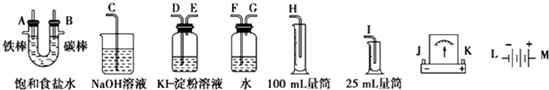
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
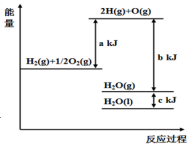
| A. | 1 mol H2(g)与$\frac{1}{2}$ mol O2(g)所具有的总能量比1 mol H2O(g)所具有的总能量高 | |
| B. | H2O(g)生成H2O(l)时,断键吸收的能量小于成键放出的能量 | |
| C. | 2 mol H(g)与1 mol O(g)生成1 molH2O(g)所放出的热量是b kJ | |
| D. | 液态水分解的热化学方程式为:2H2O(l)═2H2(g)+O2(g)△H=2(b+c-a)kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com