
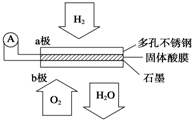
 某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见图,电池总反应可表示为:2H2+O2═2H2O,完成下列问题:
某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见图,电池总反应可表示为:2H2+O2═2H2O,完成下列问题:分析 该电池呈酸性,通入燃料氢气的电极为负极,电极反应式为H2-2e-═2H+,通入氧气的一极为电池的正极,发生还原反应,反应为O2+4e-+4H+=2H2O,电子从负极沿导线流向正极,放电时,电解质中阳离子向正极移动,结合电极方程式计算.
解答 解:①燃料电池中,通入燃料氢气的电极是负极,则a是负极,通入氧化剂的电极b是正极,电子从负极a沿导线流向正极b,
故答案为:a;b;
②通入氧气的一极为电池的正极,发生还原反应,则b是正极,电极反应式为O2+4e-+4H+=2H2O,
故答案为:O2+4e-+4H+=2H2O;
③通入燃料氢气的电极为负极,电极反应式为H2-2e-═2H+,每转移0.1mol电子,消耗H2的物质的量为0.05mol,其体积在标准状况下为1.12L;
故答案为:1.12.
点评 本题考查化学电源新型电池,燃料电池中通入燃料的电极都是负极、通入氧化剂的电极都是正极,会结合电解质溶液酸碱性书写电极反应式,题目难度中等,侧重于考查学生的分析能力和对基础知识的应用能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:推断题
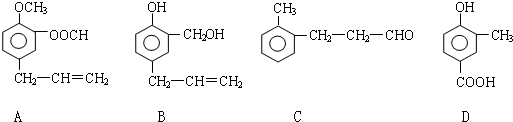
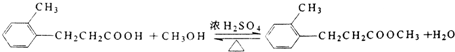 .
.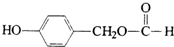 ;H:
;H: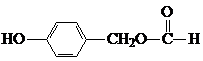 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

 .
.| 试管 编号 | 实验目的 | H2O2溶液 | 温度 | 水的 体积/mL | FeCl3溶液体积/mL | |
| 质量 分数 | 体积/mL | |||||
| Ⅰ | 为编号Ⅱ实验参照 | 12% | 5.0 | 常温 | 0 | 0 |
| Ⅱ | 温度对反应速率的影响 | 5.0 | 60℃ | 0 | 0 | |
| Ⅲ | 为编号Ⅳ实验参照 | 4.0% | 5.0 | 常温 | 0 | |
| Ⅳ | 4.0% | 5.0 | 常温 | 0 | 1.0 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,15g乙烷气体中含3.5NA个共价键 | |
| B. | 标准状况下,22.4L苯在Fe 催化条件下可与NA个Br2发生取代反应 | |
| C. | 18g2H2O中含有电子数为10NA | |
| D. | 1molN2和3molH2发生反应N2(g)+3H2(g)?2NH3(g),共有6NA个电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气 | B. | 甲烷 | C. | 乙醇 | D. | 木炭 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤ | B. | ①②③④ | C. | ①②③⑤ | D. | 全都正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若降低温度,可以加快反应速率 | |
| B. | 在上述条件下,SO2能完全转化为SO3 | |
| C. | 反应达平衡时,SO2和SO3的浓度一定相等 | |
| D. | 反应达平衡时,正反应速率和逆反应速率一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤ | B. | ②④ | C. | ①③ | D. | ①④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com