
有一无色溶液,可能含有K+、Al3+、Mg2+、NH4+、Cl-、SO42-、HCO3-、MnO4-中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量的Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的是
A.肯定有Al3+、Mg2+、NH4+、Cl- B.肯定有Al3+、Mg2+、HCO3-
C.肯定有K+、HCO3-、MnO4- D.肯定有Al3+、Mg2+、SO42-
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016届浙江省瑞安市四校高三上学期第一次联考化学试卷(解析版) 题型:填空题
(8分)A、B、C、D四种短周期元素,A元素的一种同素异形体是自然界硬度最大的单质,C与A同主族,C元素的原子序数是B的2倍,工业上以D元素的单质与石灰乳为原料制造漂白粉。按要求回答下列问题:
(1)B的原子结构示意图为 ;镁条在气体B中燃烧生成的物质是 (填化学式);
(2)A的非金属性强于C,请用一个化学反应方程式表示___________ ;
(3)元素B、D形成的化合物BD3能与水反应生成具有漂白性的物质X,写出该反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2016届湖南省益阳市高三上学期第三次模拟化学试卷(解析版) 题型:实验题
(12分)某化学研究性小组采用如下装置(夹持和加热仪器已略去)电解饱和食盐水一段时间,并通过实验测定产物的量来判断饱和食盐水的电解率。
饱和食盐水的电解率=(电解的氯化钠质量/总的氯化钠质量)×100%
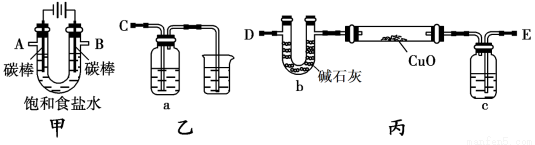
甲方案:利用甲、乙装置测定饱和食盐水的电解率,
(1)若饱和食盐水中滴有酚酞,则电解过程中甲装置中的实验现象:__________________
(2)若洗气瓶a中盛放的为足量的氢氧化钠溶液,通过测定洗气瓶a在电解前后的质量变化来计算饱和食盐水的电解率,则正确的连接顺序为 连_______(填A、B、C、等导管口),则洗气瓶a中发生反应的离子方程式为___________________
乙方案:利用甲、丙装置测定饱和食盐水的电解率,
(3)对于乙方案,有同学提出有两种方法都可测得饱和食盐水的电解率,
Ⅰ.通过测定硬质玻璃管中氧化铜固体前后质量差来计算饱和食盐水的电解率
Ⅱ.通过测定丙装置中除硬质玻璃管外的某装置前后质量差来计算饱和食盐水的电解率
①.一同学认为可以在乙方案方法Ⅱ中的装置中添加一干燥装置防止外界空气中的水蒸气的干扰,则该干燥装置应与 口连接
a.A b.B c.D d.E
②.另一同学认为乙方案的方法Ⅰ、Ⅱ测得的实验结论都不正确,你是否同意?请说明理由
丙方案:只利用甲装置测定饱和食盐水的电解率。
(4)若电解150mL饱和食盐水一段时间,测得溶液的为pH为14,求饱和食盐水的电解率
(假设电解前后溶液体积不变,饱和食盐水密度约为1.33 g/mL,溶解度为36.0g)。
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三上学期期中测试化学试卷(解析版) 题型:选择题
常温下,向0.25 mol·L-1的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验不同时刻的溶液,下列有关说法中正确的是
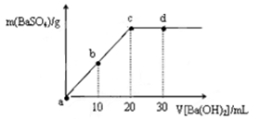
A.硫酸溶液的体积为30 mL
B.b时刻溶液中SO42-的浓度约为0.125 mol·L-1
C.d时刻溶液的pH约为13
D.溶液的导电能力:c<d=b<a
查看答案和解析>>
科目:高中化学 来源:2016届安徽省皖南八校高三上学期第一次联考化学试卷(解析版) 题型:选择题
用下列装置进行相应实验,装置正确且能达到实验目的的是

A.用图甲所示装置验证NaHCO3的不稳定性
B.用图乙所示装置干燥氨气
C.用图丙所示装置制取少量CO2气体
D.用图丁所示装置分馏石油
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省泰州市姜堰区高二上学期期中选修化学试卷(解析版) 题型:选择题
下列做法不利于“开源节流”的是
A.开发太阳能、水能、风能、地热能等新能源
B.大力开采煤、石油和天然气,以满足人们日益增长的能源需求
C.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
D.减少资源消耗,注重资源的重复使用、资源的循环再生
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二上第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.强酸跟强碱的反应热一定是中和热
B.1molC完全燃烧放热383.3kJ,其热化学方程为:
C+O2=CO2 ΔH=-383.3kJ·mol-1
C.在稀溶液中,酸与碱发生中和反应生成1 mol H2O时的反应热叫做中和热
D.表示中和热的离子方程式为:
H+(aq)+OH-(aq) H2O(l);ΔH=57.3KJ·mol-1
H2O(l);ΔH=57.3KJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高一上学期第一次月考化学试卷(解析版) 题型:选择题
相同质量的SO2和SO3它们之间的关系是
A.体积之比为5:4 B.分子数之比为1:1
C.物质的量之比为5:4 D.氧原子的个数比为2:3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com