
科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:
(12分)
已知LiH、NaH及LiAlH4都是常见的金属的氢化物,其中LiAlH4可由下列途径合
成: 4LiH + AlCl3 ![]() LiAlH4+ 3LiCl。
LiAlH4+ 3LiCl。
试探究下列相关问题
(1)下列有关说法正确的是 ▲ 。
A.该反应是氧化还原反应
B.乙醚(C2H5OC2H5)是非极性分子
C.化学性质锂与镁相似,铝与铍相似
D.LiAlH4具有还原性
(2)正在载入...
镧镍合金、铜钙合金及铈钴合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力,其中铜钙合金的晶胞结构为:
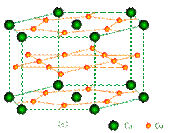
试回答下列问题
①在周期表中Ca处于周期表 ▲ 区。
②铜原子的基态核外电子排布式为: ▲ 。
③已知镧镍合金LaNin晶胞体积为9.0×10-23cm3,储氢后形成LaNinH4.5的合金(氢进入晶胞空隙,体积不变),则LaNin中,n= ▲ (填数值);氢在合金中的密度为: ▲ 。
(3)中美科学家合作发现钙和锶在C60上吸附很强,可以均匀地覆盖在C60表面上,形成M32C60。非常适于实际应用。 Ca32C60上可吸附至少92个氢分子(如图)。

有关说法正确的是 ▲ 。
A.钙的第一电离能和电负性均比锶的第一电离能小
B.C60中碳原子杂化方式为sp3
C.Ca32C60储氢是与H2发生加成反应
D.吸附相同数目氢分子时, 储氢质量分数(wt%。)Ca32C60 比Sr32C60高
查看答案和解析>>
科目:高中化学 来源: 题型:
已知LiH、NaH及LiAlH4都是常见的金属的氢化物,其中LiAlH4可由下列途径合
成: 4LiH + AlCl3 ![]() LiAlH4+ 3LiCl。
LiAlH4+ 3LiCl。
试探究下列相关问题
(1)下列有关说法正确的是 ▲ 。
A.该反应是氧化还原反应
B.乙醚(C2H5OC2H5)是非极性分子
C.化学性质锂与镁相似,铝与铍相似
D.LiAlH4具有还原性
(2)镧镍合金、铜钙合金及铈钴合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力,其中铜钙合金的晶胞结构为:

试回答下列问题
①在周期表中Ca处于周期表 ▲ 区。
②铜原子的基态核外电子排布式为: ▲ 。
③已知镧镍合金LaNin晶胞体积为9.0×10-23cm3,储氢后形成LaNinH4.5的合金(氢进入晶胞空隙,体积不变),则LaNin中,n= ▲ (填数值);氢在合金中的密度为: ▲ 。
(3)中美科学家合作发现钙和锶在C60上吸附很强,可以均匀地覆盖在C60表面上,形成M32C60。非常适于实际应用。 Ca32C60上可吸附至少92个氢分子(如图)。

有关说法正确的是 ▲ 。
A.钙的第一电离能和电负性均比锶的第一电离能小
B.C60中碳原子杂化方式为sp3
C.Ca32C60储氢是与H2发生加成反应
D.吸附相同数目氢分子时, 储氢质量分数(wt%。)Ca32C60 比Sr32C60高
查看答案和解析>>
科目:高中化学 来源:江苏省盐城中学2010届高三年级第一次化学模拟考试 题型:填空题
已知LiH、NaH及LiAlH4都是常见的金属的氢化物,其中LiAlH4可由下列途径合
成: 4LiH + AlCl3  LiAlH4+ 3LiCl。
LiAlH4+ 3LiCl。
试探究下列相关问题
(1)下列有关说法正确的是 ▲ 。
A.该反应是氧化还原反应
B.乙醚(C2H5OC2H5)是非极性分子
C.化学性质锂与镁相似,铝与铍相似
D.LiAlH4具有还原性
(2)镧镍合金、铜钙合金及铈钴合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力,其中铜钙合金的晶胞结构为:

试回答下列问题
①在周期表中Ca处于周期表 ▲ 区。
②铜原子的基态核外电子排布式为: ▲ 。
③已知镧镍合金LaNin晶胞体积为9.0×10-23cm3,储氢后形成LaNinH4.5的合金(氢进入晶胞空隙,体积不变),则LaNin中,n= ▲ (填数值);氢在合金中的密度为: ▲ 。
(3)中美科学家合作发现钙和锶在C60上吸附很强,可以均匀地覆盖在C60表面上,形成M32C60。非常适于实际应用。 Ca32C60上可吸附至少92个氢分子(如图)。

有关说法正确的是 ▲ 。
A.钙的第一电离能和电负性均比锶的第一电离能小
B.C60中碳原子杂化方式为sp3
C.Ca32C60储氢是与H2发生加成反应
D.吸附相同数目氢分子时, 储氢质量分数(wt%。)Ca32C60 比Sr32C60高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com