
几种短周期元素的原子半径及主要化合价如下表:
元素代号 X Y Z W
原子半径/pm 160 143 75 74
主要化合价 +2 +3 +3、+5、﹣3 ﹣2
下列叙述正确的是()
A. Y的最高价氧化物对应的水化物显两性
B. 一定条件下,Z单质与W的常见单质直接生成ZW2
C. X、Y元素的金属性 X<Y
D. X2+离子半径大于W2﹣离子半径
考点: 原子结构与元素周期律的关系.
专题: 元素周期律与元素周期表专题.
分析: W化合价为﹣2价,没有最高正化合价+6价,故W为氧元素;Z元素化合价为+5、+3、﹣3,Z处于ⅤA族,原子半径与氧元素相差不大,则Z与氧元素处于同一周期,则Z为氮元素;X化合价为+2价,应为周期表第ⅡA族,Y的化合价为+3价,应为周期表第ⅢA族元素,二者原子半径相差较小,可知两者位于同一周期相邻主族,由于X、Y的原子半径与W、Z原子半径相差很大,则X、Y应在第三周期,所以X为镁元素,Y为铝元素.结合元素周期律知识解答该题.
解答: 解:W化合价为﹣2价,没有最高正化合价+6价,W为氧元素;Z元素化合价为+5、+3、﹣3,Z处于ⅤA族,原子半径与氧元素相差不大,则Z与氧元素处于同一周期,则Z为氮元素;X化合价为+2价,应为周期表第ⅡA族,Y的化合价为+3价,应为周期表第ⅢA族元素,二者原子半径相差较小,可知两者位于同一周期相邻主族,由于X、Y的原子半径与W、Z原子半径相差很大,则X、Y应在第三周期,所以X为镁元素,Y为铝元素.
A.Y的最高价氧化物的水化物是氢氧化铝,属于两性氢氧化物,故A正确;
B.在放电条件下氮气与氧气可以化合生成NO,不能直接生成NO2,故B错误;
C.同周期自左而右金属性减弱,金属性X(Mg)<Y(Al),故C错误;
D.Mg2+离子、O2﹣离子电子层结构相同,核电荷数越大离子半径越小,故离子半径:Mg2+<O2﹣,故D错误,
故选:A.
点评: 本题考查元素位置结构和性质的关系及应用,题目难度中等,关键是根据原子半径、化合价推断元素,注意对元素周期律的理解掌握.


科目:高中化学 来源: 题型:
向500mL 2mol/L 的CuSO4溶液中插入一块铁片,反应片刻后取出铁片,经洗涤、烘干,称其质量比原来增重2.0g.下列说法错误的是(设反应后溶液的体积不变)()
A. 则此过程中参加反应的铁的质量是14g
B. 析出铜物质的量是0.25mol
C. 反应后溶液中溶质物质的量浓度:c(CuSO4)=1.5mol/L
D. 反应后溶液中溶质物质的量浓度:c(FeSO4)=1.5mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列结果是马虎同学回答同桌提问的答案,你认为需要改正的是()
①微粒半径:S2﹣>Cl﹣>S>Cl ②氢化物稳定性:HF>HCl>H2S>PH3③还原性:Na>Mg>Al>K ④氧化性:Cl2>S>O2>F2 ⑤酸性:H2SO4>HClO4>H2SiO3>H3PO4 ⑥得电子能力:F>Cl>Br>I.
A. 只有③ B. ③④⑤ C. ②④⑤⑥ D. ③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
在一个小烧杯里,加入约20g已研磨成粉末的氢氧化钡晶体,将小烧杯放在事先已滴有3﹣4滴水的玻璃片上,然后再加入约10g NH4Cl晶体,并立即用玻璃棒迅速搅拌.试完成下列问题: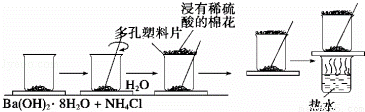
(1)写出有关反应方程式 ,该反应属于 反应.(填基本反应类型)
(2)实验中要立即用玻璃棒迅速搅拌的原因是 .
(3)如果实验中没有看到“结冰”现象,可能的原因是(列举三条)①
(4)“结冰”现象说明了该反应是吸 热(填“放”或“吸”),反应物的总能量比生成物的总能量
低(填“高”或“低”);
(5)在上述实验过程中,用浸有稀硫酸的湿棉花置于多孔塑料板上的作用是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作中错误的是()
A. 在由氢氧化铜分解制氧化铜时,要边加热边用玻璃棒搅拌
B. 用药匙或者纸槽把粉末状药品送入试管的底部
C. 过滤时玻璃棒的末端应轻轻靠在三层的滤纸上
D. 如果没有试管夹,可以临时手持试管给固体或液体加热
查看答案和解析>>
科目:高中化学 来源: 题型:
向MgSO4和Al2(SO4)3的混合溶液中,逐滴加入NaOH溶液.下列图象中,能正确表示上述反应的是(横坐标表示加入NaOH溶液的体积,纵坐标表示反应生成沉淀的质量)()
A. 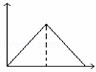 B.
B. 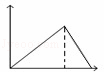 C.
C. 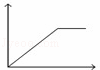 D.
D. 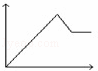
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作均要用玻璃棒,其中玻璃棒的作用及其目的相同的是()
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体.
A. ①和② B. ①和③ C. ③和④ D. ①和④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com