
维生素B1可作为辅酶参与糖的代谢,并有保护神经系统的作用。该物质的结构式为
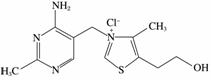
以下关于维生素B1的说法正确的是________。
A.只含σ键和π键
B.既有共价键又有离子键
C.该物质的熔点可能高于NaCl
D.该物质易溶于盐酸
(3)维生素B1晶体溶于水的过程中要克服的微粒间作用力有________。
A.离子键、共价键 B.离子键、氢键、共价键
C.氢键、范德华力 D.离子键、氢键、范德华力
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
据下列叙述,写出元素名称和核外电子排布式。
(1)A元素原子核外M层电子数是L层电子数的一半:___________。
(2)B元素原子的最外层电子数是次外层电子数的1.5倍:________________。
(3)C元素的单质在常温下可与水剧烈反应,产生的气体能使带火星的木条复燃:________________________________________。
(4)D元素的次外层电子数是最外层电子数的1/4:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
原子形成化合物时,电子云间的相互作用对物质的结构和性质会产生影响。请回答下列问题:
(1)BF3分子的立体结构为______________,NF3分子的立体结构为____________。
(2)碳原子有4个价电子,在形成化合物时价电子均参与成键,但杂化方式不一定相同。在乙烷、乙烯、乙炔和苯四种分子中,碳原子采取sp杂化的分子是____________(写结构简式,下同),采取sp2杂化的分子是__________,采取sp3杂化的分子是____________。试写出一种有机物分子的结构简式,要求同时含有三种不同杂化方式的碳原子:________________________________________________________________________。
(3)已知H2O、NH3、CH4三种分子中,键角由大到小的顺序是CH4>NH3>H2O,请分析可能的原因是________________________________________________。
(4)由于电荷的作用,阴、阳离子形成化合物时离子的电子云会发生变化,使离子键逐渐向共价键过渡。阳离子电荷数越多,阴离子半径越大时,电子云变化越大,导致所形成的化合物在水中的溶解度越小。由此可知,四种卤化银(AgF、AgCl、AgBr和AgI)在水中的溶解度由大到小的顺序为________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知a是H,b是N,c是O,d是S,a与其他元素形成的二元共价化合物中,分子中既含有极性共价键,又含有非极性共价键的化合物是________________________________(填化学式,写出两种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X的最高价氧化物对应的水化物化学式为H2XO3,Y是地壳中含量最高的元素,则XY2由固态变为气态所需克服的微粒间作用力是________;氢元素、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称________。
查看答案和解析>>
科目:高中化学 来源: 题型:
中科院国家纳米科学中心2013年11月22日宣布,该中心科研人员在国际上首次“拍”到氢键的“照片”,实现了氢键的实空间成像,为“氢键的本质”这一化学界争论了80多年的问题提供了直观证据。这不仅将人类对微观世界的认识向前推进了一大步,也为在分子、原子尺度上的研究提供了更精确的方法。下列说法中正确的是( )
A.正是氢键的存在,冰能浮在水面上
B.氢键是自然界中最重要、存在最广泛的化学键之一
C.由于氢键的存在,沸点:HCl>HBr>HI>HF
D.由于氢键的存在,水分子中氢氧键角是104.5°
查看答案和解析>>
科目:高中化学 来源: 题型:
某航空站安装了一台燃料电池,该电池可同时提供电和水蒸气。所用燃料为氢气,电解质为熔融的碳酸钾。已知该电池的总反应为2H2+O2===2H2O,正极反应为O2+2CO2+4e-===2CO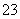 ,则下列推断正确的是 ( )。
,则下列推断正确的是 ( )。
A.负极反应为H2+2OH--2e-===2H2O
B.该电池可在常温或高温时进行工作,对环境具有较强的适应性
C.该电池供应2 mol水蒸气,同时转移2 mol电子
D.放电时负极有CO2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为元素周期表的一部分,请回答下列有关问题:
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
(1)⑤和⑧的元素符号是________和________。
(2)表中最活泼的金属是________,非金属性最强的元素是________(填写元素符号)。
(3)表中能形成两性氢氧化物的元素是________,分别写出该元素的氢氧化物与⑥、⑨的最高价氧化物对应水化物反应的化学方程式:________________________,______________________________。
(4)请设计一个实验方案,比较⑦、⑩单质氧化性的强弱:
___________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com