
【题目】水壶长时间使用后,会形成一层水垢(主要成分为CaCO3).厨房中的下列物质可用来清除水垢的是( )
A.白醋
B.食盐
C.料酒
D.小苏打
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】25 ℃时,在20 mL 0.1 mol/L NaOH溶液中加入0.2 mol/L CH3COOH溶液,所加入溶液的体积(v)和混合液中pH变化关系的曲线如下图所示,若B点的横坐标a=10,下列分析的结论正确的是( )
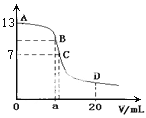
A. 在B点有:c(Na+)=c(CH3COO-)
B. 对曲线上A、B间任何一点,溶液中都有:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
C. C点时,c(CH3COO-)=c(Na+)>c(H+)=c(OH-)
D. D点时,c(CH3COO-)+c(CH3COOH)=c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2·6H2O的流程如下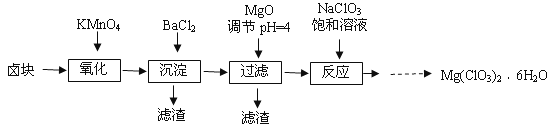
已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
②四种化合物的溶解度(S)随温度(T)变化曲线如图所示。
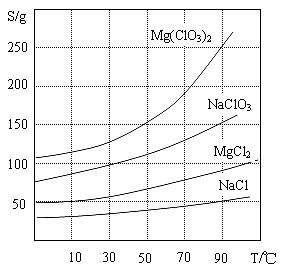
(1)过滤所需要的主要玻璃仪器有 ,
(2)加入BaCl2的目的是 ,加MgO后过滤所得滤渣的主要成分为 。
(3)加入NaClO3饱和溶液后发生反应的化学方程式为 ,再进一步制取Mg(ClO3)2·6H2O的实验步骤依次为:①蒸发结晶;② ;洗涤;③将滤液冷却结晶;④过滤、洗涤。
(4)产品中Mg(ClO3)2·6H2O含量的测定:(已知Mg(ClO3)2·6H2O的摩尔质量为299g/mol)
步骤1:准确称量3.50 g产品配成100 mL溶液。
步骤2:取10.00 mL于锥形瓶中,加入10.00 mL稀硫酸和20 .00mL 1.000 mol·L-1的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100 mol/L K2Cr2O7 溶液滴定剩余的Fe2+至终点。反应的方程式为: Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。
步骤4:将步骤2、3重复两次,平均消耗K2Cr2O7 溶液15.00 mL。
①写出步骤2中发生反应的离子方程式: ;
② 产品中Mg(ClO3)2·6H2O的质量分数为 。(保留到小数点后一位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种元素,它们原子的核电荷数均小于18,且依次增大,A原子核内仅有一个质子;B原子的电子总数与D原子的最外层电子数相等;A原子与B原子最外层电子数之和与C原子的最外层电子数相等;D原子有两个电子层,最外层龟子数是次外层电子数的3倍。
(1)试推断它们各是什么元素? 写出它们的元素符号:A______,B________,C_______,D_______。
(2)甲、乙、丙、丁是由以上四种元素中的几种组成的10 电子微粒;
①甲为分子,且能刻蚀玻璃,则甲的化学式为______
②乙为气体,且遇到无色酚酞溶液变成红色,则乙的化学式为_______
③丙为阳离子,丁为阴离子,且丙和丁在加热条件下生成的两种物质也是10电子微粒,请写出该反应的离子方程式_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.分子式为C2H6O的有机化合物性质相同
B.相同条件下,等质量的碳按a、b两种途径完全转化,途径a比途径b放出更多热能途径a:C ![]() CO+H2
CO+H2 ![]() CO2+H2O
CO2+H2O
途径b:C ![]() CO2
CO2
C.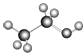 可以表示乙醇分子的球棍模型
可以表示乙醇分子的球棍模型
D.![]() :既可以表示甲烷分子,也可以表示四氯化碳分子
:既可以表示甲烷分子,也可以表示四氯化碳分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种主族元素的原子序数依次增大,且均小于18.A原子的最外层电子比B原子的最外层电子少2个,B原子的质子数是其电子层数的4倍.A、B、C三种元素能结合成化合物C2AB3,在lmolC2AB3中共有52mol电子。D元素的单质0.5mol与酸全部反应时,有9.03×1023个电子转移。E元素的单质是一种黄绿色气体,水溶液具有漂白性。试填写下列空白:
(l)写出元素A 和E 的名称:A , E 。
(2)元素B在周期表中的位置为第二周期 族.
(3)由元素B、C形成的一种化合物可以作为呼吸面具的供氧剂,该化合物为含有 键(填“极性”或“非极性”)的 化合物(填“离子”或“共价”) ,写出该化合物的电子式 。
(4)写出C、D两种元素对应的最高价氧化物的水化物相互反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E五种可溶性强电解质,它们在水中可电离产生下列离子(各离子不重复):阳离子:H+、Na+、Al3+、Ag+、Ba2+ 阴离子:OH﹣、Cl﹣、CO32﹣、NO3﹣、SO42﹣
已知:①A、B两溶液呈碱性,C、D、E溶液呈酸性.
②向E溶液中逐滴滴加B溶液至过量,沉淀量先增加后减少但不消失.
③D溶液与另外四种溶液反应都能产生沉淀.
请回答下列问题:
(1)写出A与D的化学式:A , D .
(2)写出A与E溶液反应的离子方程式: .
(3)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(1)△H=﹣akJmol﹣1 . 请写出表示相同条件下B与C的稀溶液反应的中和热的热化学方程式: .
(4)若25℃时,C、E及醋酸三种溶液的pH=4,则E和C溶液中由水电离出的c(H+)的比是;将C与醋酸混合,醋酸的电离程度将(填“增大”“不变”或“减小”).
(5)用惰性电极电解0.1molL﹣1 D与0.1molL﹣1C各100mL混合后的溶液,电解一段时间后,阴极质量(填“增大”“不变”或“减小”,下同);溶液的pH .
(6)向(5)中所得溶液中加入足量铁粉,则所能溶解的铁粉质量为g.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com