
| A. | 铜片插A硝酸银溶液中:Cu+Ag+═Cu2++Ag | |
| B. | 盐酸滴入澄清石灰水:Ca(OH)2+2H+═Ca2++2H2O | |
| C. | 将金属Na加入冷水中:2Na+2H2O═2Na+++2OH-+H2↑ | |
| D. | 向含0.5molFeBr2的溶液中通入0.5molC12:2Fe2++C12═2Fe3++2C1- |
分析 A.电荷不守恒;
B.澄清石灰水中氢氧化钙应拆成离子形式;
C.二者反应生成氢氧化钠和氢气;
D.二价铁离子全部被氧化,溴离子一半被氧化.
解答 解:A.铜片插A硝酸银溶液中,离子方程式:Cu+2Ag+═Cu2++2Ag,故A错误;
B.盐酸滴入澄清石灰水,离子方程式:OH-+H+═H2O,故B错误;
C.将金属Na加入冷水中,离子方程式:2Na+2H2O═2Na++2OH-+H2↑,故C正确;
D.向含0.5molFeBr2的溶液中通入0.5molC12,离子方程式:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-,故D错误;
故选:C.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意离子反应遵循客观事实、遵循电荷守恒规律,注意氧化还原反应先后规律,题目难度不大.


科目:高中化学 来源: 题型:解答题
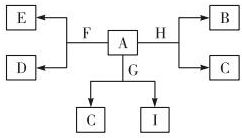 如图是中学化学某些物质之间的相互转化关系,已知A是种常见的液态化合物,C、D、G、H均为单质,G、H形成的合金是当前使用量最大的一种合金,B是黑色固体.
如图是中学化学某些物质之间的相互转化关系,已知A是种常见的液态化合物,C、D、G、H均为单质,G、H形成的合金是当前使用量最大的一种合金,B是黑色固体.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温常压下,71g Cl2所含原子数为NA | |
| B. | 标准状况下,22.4L氦气中含有的原子数为2NA | |
| C. | 在非标准状况下,1mol任何气体的体积不可能是22.4L | |
| D. | 常温常压下,32g O2和O3混合气体中含有原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把苯甲酸、甲醇、稀硫酸混合置于有回流设备的装置中,加热,合成苯甲酸甲酯 | |
| B. | 把苯和少量溴水及少量铁屑放在用带导管的瓶塞塞紧瓶口的烧瓶里,反应制取溴苯 | |
| C. | 把醋酸钠晶体(CH3COONa•3H2O)与干燥的碱石灰按一定比例混合后,加热,制取甲烷 | |
| D. | 把浓硝酸、浓硫酸、苯的混合液放在60℃的水浴中反应,制取硝基苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应物的总能量低于生成物的总能量时,一定不能自发进行反应 | |
| B. | 已知:CH4(g)+$\frac{3}{2}$O2(g)═2H2O(l)+CO(g)△H,则△H表示CH4的燃烧热 | |
| C. | 恒温恒压时,将2 mol A和1 mol B投入密闭容器中,发生反应:2A(g)+B(g)?2C(g),充分反应后测得放出的热量为Q kJ,则该反应的△H=-Q kJ/mol | |
| D. | 由4P(s,红磷)═P4(s,白磷)△H=+139.2 kJ/mol,可知红磷比白磷稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. |  分散系的分类 | B. | 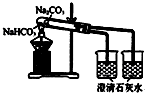 比较Na2CO3、NaHCO3的稳定性 | ||
| C. | 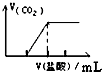 向Na2CO3溶液中逐滴滴入盐酸 | D. | 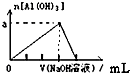 向Al溶液中滴加过量的NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com