
����Ŀ��ij�¶�ʱ����һ���ݻ�Ϊ2L���ܱ������У�X��Y��Z�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ�� 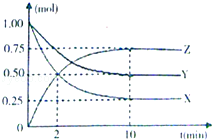
����ͼ�����ݣ�����������⣺
��1���÷�Ӧ�Ļ�ѧ������
��2����Ӧ��ʼ��2min������Z��ƽ����Ӧ����Ϊ��
��3����X��Y��Z��Ϊ���壬��Ӧ��ʼʱ��ƽ����ѹǿ֮���� ��
��4���ﵽƽ�������˵������ȷ����
A.X��Y��Z��Ũ��֮����1��2��3
B.X���������ʺ�Y�������������
C.Z��Ũ�ȱ��ֲ���
D.�����¶����´ﵽƽ�⣬Z��Ũ�ȼ�С����÷�ӦΪ���ȷ�Ӧ��
���𰸡�
��1��3X+2Y?3Z
��2��0.125mol/��L��min��
��3��4��3
��4��BD
����������1������ͼ֪�����ŷ�Ӧ�Ľ��У�X��Y�����ʵ������ٶ�Z�����ʵ�����������X��Y�Ƿ�Ӧ�Z�������10minʱ��Ӧ�ﵽƽ��״̬����μӷ�Ӧ�ġ�n��X��=��1.00��0.25��mol=0.75mol����n��Y��=��1.00��0.50��mol=0.50mol����n��Z��=��0.75��0��mol=0.75mol��ͬһ���淴Ӧ��ͬһʱ����ڲμӷ�Ӧ�ĸ����ʵ����ʵ���֮�ȵ����������֮�ȣ�����X��Y��Z�ļ�����֮��=0.75mol��0.50mol��0.75mol=3��2��3�����Ը÷�Ӧ����ʽΪ3X+2Y3Z�� ���Դ��ǣ�3X+2Y3Z����2��0��2min��Z��ƽ����Ӧ����= ![]() =
= ![]() =0.125mol/��L��min�������Դ��ǣ�0.125mol/��L��min������3�����º��������£������ѹǿ֮�ȵ��������ʵ���֮�ȣ���Ӧǰ����������ʵ���=1.00mol��2=2.00mol��ƽ�������������ʵ���=��0.25+0.50+0.75��mol=1.50mol�����Է�Ӧ��ʼʱ��ƽ����ѹǿ֮��=2.00mol��1.50mol=4��3�����Դ��ǣ�4��3����4��A����ͬ�����У�X��Y��Z��Ũ��֮�ȵ��������ʵ���֮��=0.25mol��0.50mol=0.75mol=1��2��3����A��ȷ��B���÷�Ӧ��X��Y�ļ�����֮��Ϊ3��2����X������������Y����������֮��Ϊ3��2ʱ�÷�Ӧ�ﵽƽ��״̬�����Ե�X���������ʺ�Y�������������ʱ�÷�Ӧû�дﵽƽ��״̬����B����
=0.125mol/��L��min�������Դ��ǣ�0.125mol/��L��min������3�����º��������£������ѹǿ֮�ȵ��������ʵ���֮�ȣ���Ӧǰ����������ʵ���=1.00mol��2=2.00mol��ƽ�������������ʵ���=��0.25+0.50+0.75��mol=1.50mol�����Է�Ӧ��ʼʱ��ƽ����ѹǿ֮��=2.00mol��1.50mol=4��3�����Դ��ǣ�4��3����4��A����ͬ�����У�X��Y��Z��Ũ��֮�ȵ��������ʵ���֮��=0.25mol��0.50mol=0.75mol=1��2��3����A��ȷ��B���÷�Ӧ��X��Y�ļ�����֮��Ϊ3��2����X������������Y����������֮��Ϊ3��2ʱ�÷�Ӧ�ﵽƽ��״̬�����Ե�X���������ʺ�Y�������������ʱ�÷�Ӧû�дﵽƽ��״̬����B����
C����Z��Ũ�ȱ��ֲ���ʱ�����淴Ӧ������ȣ����淴Ӧ�ﵽƽ��״̬����C��ȷ��
D�������¶����´ﵽƽ�⣬Z��Ũ�ȼ�С��ƽ�������ƶ��������¶�ƽ�������ȷ����ƶ�����������Ӧ�Ƿ��ȷ�Ӧ����D����
��ѡBD��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ӫ�������У����ڸ߷��ӵ���
A. ���� B. ��֬ C. ������ D. ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1molL��1������Һ�ĺ�����
A. 1Lˮ���ܽ�1mol����
B. ��98gŨ��������ˮ���1L��Һ
C. 1L��Һ�к�1mol H2SO4����
D. ָ1L������Һ������98g����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼװ�ý���ʵ�飬�ס��������о�Ϊ1 mol��L��1��AgNO3��Һ��A��B��ΪAg�缫��ʵ�鿪ʼʱ�ȱպ�K1���Ͽ�K2��һ��ʱ��Ͽ�K1���պ�K2���γ�Ũ���أ�������ָ��ƫת(Ag��Ũ��Խ��������Խǿ)������˵������ȷ����(����)

A. �պ�K1���Ͽ�K2��A�缫����
B. �պ�K1���Ͽ�K2���ҳ���ҺŨ������
C. �Ͽ�K1���պ�K2��A�缫����������Ӧ
D. �Ͽ�K1���պ�K2��NO![]() ��B�缫�ƶ�
��B�缫�ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�������ij��Ӧ��M��N�����ʵ����淴Ӧʱ��仯����������ͼ���� �б�������ȷ���ǣ� �� 
A.t3ʱ������Ӧ���ʴ����淴Ӧ����
B.t2ʱ�����淴Ӧ������ȣ���Ӧ�ﵽƽ��״̬I �ѷ�Ӧ��
C.��ѧ����ʽΪ��2M=N
D.t1ʱ��N��Ũ����MŨ�ȵ�2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���绯ѧװ������ͼ�����ڸ�װ��˵����ȷ���ǣ� ��
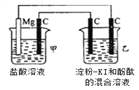
A. �׳���Mg��Ϊ�������缫��ӦʽΪ��Mg-2e-�TMg2+
B. �׳���C�缫����������Ӧ
C. �ҳ��н���ѧ��ת��Ϊ����
D. �ҳ����ʯī�缫�����������Ҳ�ʯī�缫�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ���У�����ȡ�ķ��뷽�����Ӧԭ������ȷ���ǣ� ��
ѡ�� | Ŀ�� | ���뷽�� | ԭ�� |
A�� | ��������ˮ�еĵ� | �Ҵ���ȡ | �����Ҵ��е��ܽ�Ƚϴ� |
B�� | ���������������Ҵ� | ��Һ | �����������Ҵ����ܶȲ�ͬ |
C�� | ��ȥKNO3�����л��ӵ�NaCl | �ؽᾧ | NaCl��ˮ�е��ܽ�Ⱥܴ� |
D�� | ��ȥ�����е����� | ���� | ���������ѵķе����ϴ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Q��R��T��M��W���ֶ�����Ԫ�������ڱ��е����λ����ͼ��ʾ������M��ԭ��������R��ԭ��������2��������˵����ȷ���ǣ� �� ![]()
A.MW6�и�ԭ�Ӻ��������8�����ȶ��ṹ
B.Q��W�ĵ������ӵĺ�����������
C.����Ԫ�ؾ����γ��⻯��
D.W���⻯��ˮ��Һ������ǿ��˵��W�ķǽ�����������Ԫ������ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���йغϽ����������ȷ���� �� ��
A. �Ͻ���۵�����ĸ��ɷݽ������۵�� B. �Ͻ��Ӳ�Ⱥ�ǿ��һ��ȴ�������
C. �Ͻ�һ���ǽ����ۺ϶��ɵ����� D. Ӳ������ͭ�־�Ϊ�Ͻ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com