
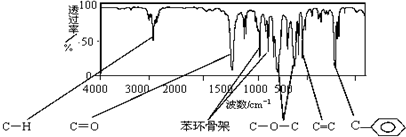
 £®
£®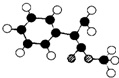 £ØĶ¼ÖŠĒņÓėĒņÖ®¼äĮ¬Ļß±ķŹ¾µ„¼ü»ņĖ«¼ü£©£®
£ØĶ¼ÖŠĒņÓėĒņÖ®¼äĮ¬Ļß±ķŹ¾µ„¼ü»ņĖ«¼ü£©£®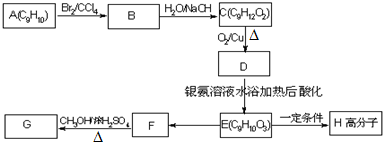
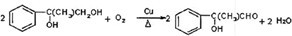 £®E”śH
£®E”śH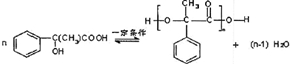 £®
£®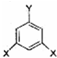 £ØĘäÖŠX”¢Y¾ł²»ĪŖH£©£¬ŹŌŠ“³ö·ūŗĻÉĻŹöĶØŹ½ĒŅÄÜ·¢ÉśŅų¾µ·“Ó¦ŗĶÓöĀČ»ÆĢśČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦µÄ2ÖÖĪļÖŹµÄ½į¹¹¼ņŹ½
£ØĘäÖŠX”¢Y¾ł²»ĪŖH£©£¬ŹŌŠ“³ö·ūŗĻÉĻŹöĶØŹ½ĒŅÄÜ·¢ÉśŅų¾µ·“Ó¦ŗĶÓöĀČ»ÆĢśČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦µÄ2ÖÖĪļÖŹµÄ½į¹¹¼ņŹ½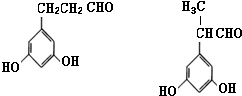 £®
£® ·ÖĪö £Ø1£©Čā¹šĖį¼×õ„µÄ·Ö×ÓŹ½ĪŖC10H10O2£¬²»±„ŗĶ¶ČĪŖ $\frac{2”Į10+2-10}{2}$=6£¬·Ö×ÓÖŠÖ»ŗ¬ÓŠ1øö±½»·£¬±½»·ÉĻÖ»ÓŠŅ»øöČ”“ś»ł£¬¹Ź»¹ŗ¬ÓŠ1øöC=CĖ«¼ü£¬Čā¹šĖį¼×õ„µÄŗĖ“Ź²ÕńĒāĘ×Ę×Ķ¼ÓŠ6øö·å£¬ĘäĆ껿֮±ČĪŖ1£ŗ2£ŗ2£ŗ1£ŗ1£ŗ3£¬¹ŹČā¹šĖį¼×õ„µÄ½į¹¹¼ņŹ½ĪŖ£ŗ £»
£»
£Ø2£©Óɽį¹¹Ä£ŠĶæÉÖŖGĪŖ £¬ŌņFĪŖ
£¬ŌņFĪŖ £¬øł¾ŻĢ¼Į“½į¹¹æÉÖŖAĪŖ
£¬øł¾ŻĢ¼Į“½į¹¹æÉÖŖAĪŖ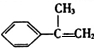 £¬BĪŖ
£¬BĪŖ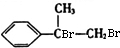 £¬CĪŖ
£¬CĪŖ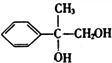 £¬DĪŖ
£¬DĪŖ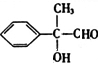 £¬EĪŖ
£¬EĪŖ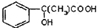 £¬HĪŖ
£¬HĪŖ £¬½įŗĻÓŠ»śĪļµÄ½į¹¹ŗĶŠŌÖŹ½ā“šøĆĢā£®
£¬½įŗĻÓŠ»śĪļµÄ½į¹¹ŗĶŠŌÖŹ½ā“šøĆĢā£®
½ā“š ½ā£ŗ£Ø1£©Čā¹šĖį¼×õ„µÄ·Ö×ÓŹ½ĪŖC10H10O2£¬²»±„ŗĶ¶ČĪŖ $\frac{2”Į10+2-10}{2}$=6£¬·Ö×ÓÖŠÖ»ŗ¬ÓŠ1øö±½»·£¬±½»·ÉĻÖ»ÓŠŅ»øöČ”“ś»ł£¬¹Ź»¹ŗ¬ÓŠ1øöC=CĖ«¼ü£¬Čā¹šĖį¼×õ„µÄŗĖ“Ź²ÕńĒāĘ×Ę×Ķ¼ÓŠ6øö·å£¬ĘäĆ껿֮±ČĪŖ1£ŗ2£ŗ2£ŗ1£ŗ1£ŗ3£¬¹ŹČā¹šĖį¼×õ„µÄ½į¹¹¼ņŹ½ĪŖ£ŗ £¬
£¬
¹Ź“š°øĪŖ£ŗ
£Ø2£©Óɽį¹¹Ä£ŠĶæÉÖŖGĪŖ £¬ŌņFĪŖ
£¬ŌņFĪŖ £¬øł¾ŻĢ¼Į“½į¹¹æÉÖŖAĪŖ
£¬øł¾ŻĢ¼Į“½į¹¹æÉÖŖAĪŖ £¬BĪŖ
£¬BĪŖ £¬CĪŖ
£¬CĪŖ £¬DĪŖ
£¬DĪŖ £¬EĪŖ
£¬EĪŖ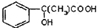 £¬HĪŖ
£¬HĪŖ £¬
£¬
¢ŁEĪŖ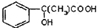 £¬ŗ¬ÓŠµÄ¹ŁÄÜĶÅĪŖōĒ»ł”¢ōČ»ł£¬
£¬ŗ¬ÓŠµÄ¹ŁÄÜĶÅĪŖōĒ»ł”¢ōČ»ł£¬
¹Ź“š°øĪŖ£ŗōĒ»ł”¢ōČ»ł£»
¢ŚAĪŖ £¬Óėäå·¢Éś¼Ó³É·“Ӧɜ³ÉB£¬EĪŖ
£¬Óėäå·¢Éś¼Ó³É·“Ӧɜ³ÉB£¬EĪŖ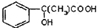 £¬EŌŚÅØĮņĖį¼ÓČČĢõ¼žĻĀ·¢ÉśĻūČ„·“Ó¦µĆF£¬
£¬EŌŚÅØĮņĖį¼ÓČČĢõ¼žĻĀ·¢ÉśĻūČ„·“Ó¦µĆF£¬
¹Ź“š°øĪŖ£ŗ¼Ó³É·“Ó¦£»ÅØĮņĖį¼ÓČČ£»
¢ŪCĪŖ £¬·¢Éś“ß»ÆŃõ»ÆÉś³É
£¬·¢Éś“ß»ÆŃõ»ÆÉś³É £¬·“Ó¦µÄ·½³ĢŹ½ĪŖ
£¬·“Ó¦µÄ·½³ĢŹ½ĪŖ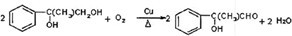 £¬EĪŖ
£¬EĪŖ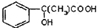 £¬ŗ¬ÓŠ-OHŗĶ-COOH£¬æÉ·¢ÉśĖõ¾Ū·“Ó¦£¬·“Ó¦µÄ·½³ĢŹ½ĪŖ
£¬ŗ¬ÓŠ-OHŗĶ-COOH£¬æÉ·¢ÉśĖõ¾Ū·“Ó¦£¬·“Ó¦µÄ·½³ĢŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ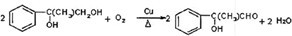 £»
£» £»
£»
¢ÜEĪŖ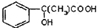 £¬EµÄĶ¬·ÖŅģ¹¹Ģ壬ĘäÖŠÓŠŅ»ĄąæÉÓĆĶØŹ½
£¬EµÄĶ¬·ÖŅģ¹¹Ģ壬ĘäÖŠÓŠŅ»ĄąæÉÓĆĶØŹ½ 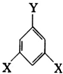 ±ķŹ¾£ØĘäÖŠX”¢Y¾ł²»ĪŖH£©£¬ĒŅÄÜ·¢ÉśŅų¾µ·“Ó¦µÄĖÄÖÖĪļÖŹµÄ½į¹¹¼ņĪŖ
±ķŹ¾£ØĘäÖŠX”¢Y¾ł²»ĪŖH£©£¬ĒŅÄÜ·¢ÉśŅų¾µ·“Ó¦µÄĖÄÖÖĪļÖŹµÄ½į¹¹¼ņĪŖ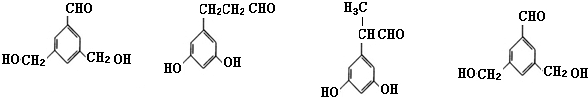 £¬ÓöĀČ»ÆĢśČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦µÄ2ÖÖĪļÖŹĪŖ
£¬ÓöĀČ»ÆĢśČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦µÄ2ÖÖĪļÖŹĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £®
£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄĶʶĻ£¬ĪŖøßæ¼³£¼ūĢāŠĶ£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦µÄ漲飬ĢāÄæÄѶČÖŠµČ£¬±¾Ģā²ąÖŲÓŚÓŠ»śĪļµÄ½į¹¹”¢ŠŌÖŹµÄ漲飬עŅāøł¾ŻÓŠ»śĪļ½į¹¹Ä£ŠĶÅŠ¶ĻGµÄ½į¹¹£¬ĪŖ½ā“šøĆĢāµÄ¹Ų¼ü£¬ŅŖĢŲ±š×¢ÖŲÓŠ»śĪļ¹ŁÄÜĶÅŠŌÖŹµÄ°ŃĪÕ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼×ĶéŹĒŅ»ÖÖ»ĘĀĢÉ«ĘųĢå | |
| B£® | ¼×ĶéŹĒŅ»ÖÖÓŠ³ōĪ¶µÄĘųĢå | |
| C£® | ŹÕ¼Æ¼×Ķ鏱³£ÓĆÅÅĖ®·Ø£¬ŹĒŅņĪŖ¼×ĶéµÄĆܶČÓėæÕĘųµÄĆܶČĻą½ü | |
| D£® | ¼×ĶéÄÜÓĆÅÅĖ®·ØŹÕ¼ÆŹĒŅņĪŖ¼×ĶéÄŃČÜÓŚĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĢĒĄą”¢ÓĶÖ¬”¢µ°°×ÖŹ¶¼ŹĒøß·Ö×Ó»ÆŗĻĪļ | |
| B£® | 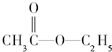 Óė H$\stackrel{18}{2}$O·¢ÉśĖ®½ā·“Ó¦£¬Éś³ÉµÄ²śĪļÖŠ18O“ęŌŚÓŚŅŅ“¼ÖŠ Óė H$\stackrel{18}{2}$O·¢ÉśĖ®½ā·“Ó¦£¬Éś³ÉµÄ²śĪļÖŠ18O“ęŌŚÓŚŅŅ“¼ÖŠ | |
| C£® | ³żČ„ŅŅĖįŅŅõ„ÖŠ»ģÓŠµÄŅŅĖį£¬æÉŅŌ¼ÓČėŅŅ“¼¼ĢŠųõ„»Æ | |
| D£® | ÓĶÖ¬²»¹ÜŌŚÄÄÖÖĢõ¼žĻĀĖ®½ā¶¼Éś³É±ūČż“¼£ØøŹÓĶ£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
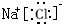 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
 »ÆѧŹ½ĪŖC2H6OµÄ»ÆŗĻĪļA¾ßÓŠČēĻĀŠŌÖŹ£ŗ
»ÆѧŹ½ĪŖC2H6OµÄ»ÆŗĻĪļA¾ßÓŠČēĻĀŠŌÖŹ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
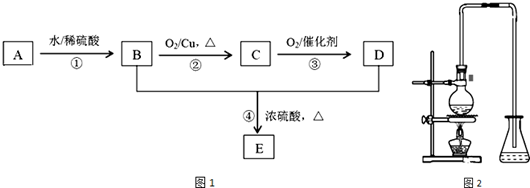
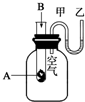 ĪŖĮĖŃŠ¾æ»Æѧ·“Ó¦A+BØTC+DµÄÄÜĮæ±ä»ÆĒéæö£¬Ä³Ķ¬Ń§Éč¼ĘĮĖČēĶ¼ĖłŹ¾×°ÖĆ£®µ±ĻņŹ¢ÓŠAµÄŹŌ¹ÜÖŠµĪ¼ÓŹŌ¼ĮBŹ±£¬æ“µ½UŠĪ¹ÜÖŠ¼×“¦ŅŗĆęĻĀ½µŅŅ“¦ŅŗĆęÉĻÉż£®ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
ĪŖĮĖŃŠ¾æ»Æѧ·“Ó¦A+BØTC+DµÄÄÜĮæ±ä»ÆĒéæö£¬Ä³Ķ¬Ń§Éč¼ĘĮĖČēĶ¼ĖłŹ¾×°ÖĆ£®µ±ĻņŹ¢ÓŠAµÄŹŌ¹ÜÖŠµĪ¼ÓŹŌ¼ĮBŹ±£¬æ“µ½UŠĪ¹ÜÖŠ¼×“¦ŅŗĆęĻĀ½µŅŅ“¦ŅŗĆęÉĻÉż£®ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū¢Ü | B£® | ¢Ś¢Ü | C£® | ¢Ł¢Ū | D£® | ¢Ł¢Ś |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | £Ø1£©ŗĶ£Ø6£© | B£® | £Ø3£©ŗĶ£Ø4£© | C£® | £Ø2£©ŗĶ£Ø4£© | D£® | £Ø2£©ŗĶ£Ø5£© |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com