
根据下列实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 取少量待检验溶液,向其中加入少量新制氯水,再滴加KSCN溶液,溶液呈血红色 | 待测液中含有Fe3+ |
B | 室温下,向浓度均为0.1 mol·L-1的BaCl2和CaCl2混合溶液中滴加Na2SO4溶液,出现白色沉淀。 | Ksp(BaSO4)< Ksp(CaSO4) |
C | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色 | Fe3+的氧化性比I2的强 |
D | 室温下,用pH试纸测得:0.1mol·L-1 Na2SO3溶液的pH约为10;0.1mol·L-1 NaHSO3溶液的pH约为5 | HSO3-结合H+的能力比SO32-的强 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年江苏省高一上期中化学卷(解析版) 题型:推断题
(1)现有①硫酸②酒精③液氨④纯碱⑤熔融的氢氧化钠⑥水银⑦三氧化硫⑧澄清石灰水等物质中,属于盐的是(填序号,下同) ,属于酸性氧化物的是 ,能导电的是 ,属于电解质的是 。
(2)有甲、乙、丙三种元素,甲元素M层的电子数是其K层的电子数的1/2,乙元素原子核内无中子,丙元素原子核内有8个质子。
①写出丙元素的元素符号 。
②写出甲、乙、丙三种元素组成的化合物在水中的电离方程式 。
③画出甲元素的原子结构示意图 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二上期中必修化学卷(解析版) 题型:选择题
目前我国许多城市定期公布空气质量报告,在空气质量报告中,一般不涉及( )
A.SO2 B.NO2 C.CO2 D.可吸入颗粒物
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江双鸭山一中高二上期中化学卷(解析版) 题型:选择题
能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的操作是
A.向水中投入一小块金属钠 B.向水中通入二氧化硫气体
C.将水加热煮沸 D.向水中加硫酸钠晶体
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江双鸭山一中高二上期中化学卷(解析版) 题型:选择题
下面是四位同学在学习“化学反应的速率和化学平衡”一章后,联系工业生产实际所发表的观点,你认为不正确的是
A.使用催化剂,可加快反应速率,目的是提高生产效率
B.使用冰箱保存食物,是利用了化学反应速率理论
C.化学反应速率理论是研究怎样提高原料转化率
D.化学平衡理论是研究怎样使用有限原料多出产品
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆一中高二上11月月考化学卷(解析版) 题型:选择题
相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g) 2NH3(g)△H=﹣92.6kJ/mol.实验测得起始、平衡时的有关数据如下表:
2NH3(g)△H=﹣92.6kJ/mol.实验测得起始、平衡时的有关数据如下表:
容器 编号 | 起始时各物质的物质的量/mol | 达平衡时体系能量的变化 | ||
N2 | H2 | NH3 | ||
① | 1 | 3 | 0 | 放出热量:23.15 kJ |
② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
下列叙述不正确的是
A.容器①、②中反应的平衡常数相等
B.平衡时,两个容器中NH3的体积分数均为1/7
C.容器②中达平衡时放出的热量Q=23.15kJ
D.若容器①体积为0.5L,则平衡时放出的热量小于23.15kJ
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆一中高二上11月月考化学卷(解析版) 题型:选择题
25℃时,在等体积的下列溶液中,发生电离的水的物质的量之比是
①pH=0的H2SO4溶液 ②0.05mol/L的Ba(OH)2溶液
③pH=10的Na2S溶液 ④pH=5的NH4NO3溶液
A.1:10:1010:109 B.1:5:5×109:5×108
C.1:20:1010:109 D.1:10:104:109
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上期中化学试卷(解析版) 题型:选择题
如图所示,纵轴表示导电能力,横轴表示所加溶液的量,下列说法正确的是
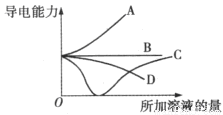
A.曲线A表示NaOH溶液中滴加稀盐酸
B.曲线B表示CH3COOH溶液中滴加KOH溶液
C.曲线C表示Ba(OH)2溶液中滴加稀硫酸
D.曲线D表示Cu(OH)2悬浊液中滴加HNO3溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上11月月考化学卷(解析版) 题型:填空题
如图所示,有T1、T2两种温度下BaSO4在水中的沉淀溶解平衡曲线如图所示,请回答下列问题:

(1)T1________T2(填“>”、“<”或“=”),T2温度时时Ksp(BaSO4)=___________。
(2)根据T1温度时BaSO4的沉淀溶解平衡曲线,判断下列说法正确的是________(填序号)。
A.加入Na2SO4可由a点变为b点
B.在T1曲线上方区域(不含曲线)的任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能由d点变为T1曲线上a、b之间的某一点(不含a、b)
D.升温可由b点变为d点
(3)T2时, 现有0.2mol的BaSO4沉淀,每次用1L饱和Na2CO3溶液(浓度为1.7mol/L)处理.若使BaSO4中的SO42-全部转化到溶液中,需要反复处理________次。[提示:BaSO4(s)+CO32-(aq)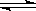 BaCO3(s)+SO42- (aq),K= Ksp(BaSO4/ Ksp(BaCO3);Ksp(BaCO3)=1.19×10-7]
BaCO3(s)+SO42- (aq),K= Ksp(BaSO4/ Ksp(BaCO3);Ksp(BaCO3)=1.19×10-7]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com