
【题目】六氟磷酸钠(NaPF6)极易溶于水,可溶于乙醇、丙酮等有机溶剂,可作高能钠电池的电解质。工业上以氟磷灰石[Ca5(PO4)3F]、NaCl为主要原料,制备六氟磷酸钠的工艺流程如下:
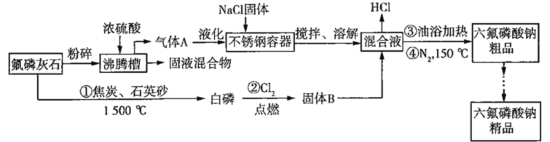
已知:HF的熔点为-83 ℃,沸点为19.5 ℃。回答下列问题:
(1)氟磷灰石粉碎的目的是_______________。
(2)HF液化时产生的二聚物(HF)2能发生微弱的电离,与NaCl反应生成NaHF2,请写出该二聚物的电离方程式:________。
(3)为避免废水NaH2PO4的污染,常在其中加入石灰,将磷元素全部转化成磷酸钙,进行回收利用。已知常温下Ksp[Ca3(PO4)2]=1.96×10-29,当处理后的废水c(Ca2+)=1.0×10-5 mol/L时,则溶液中c(![]() )=___________mol/L。
)=___________mol/L。
(4)操作③油浴加热目的是________。
(5)反应①中除生成白磷(P4)外,还产生SiF4和一种还原性气体,写出该反应的化学方程式:______。
(6)六氟磷酸钠粗品的提纯:将六氟磷酸钠粗品(杂质主要是微量铁盐)溶于一定量乙醇中,加入适量5%的NaOH甲醇溶液,使溶液保持碱性,离心将不溶杂质除去。通过______(填操作方法)将溶剂回收,减压条件下结晶,得到NaPF6·H2O,干燥得到无水盐。
【答案】增大反应物的接触面积,加快反应速率 (HF)2H++![]() 或 2HFH++
或 2HFH++![]() 1.4×10-7 除去残留的氟化氢 4Ca5(PO4)3F+21SiO2+30C
1.4×10-7 除去残留的氟化氢 4Ca5(PO4)3F+21SiO2+30C![]() 20CaSiO3+3P4+SiF4↑+30CO↑ 蒸馏
20CaSiO3+3P4+SiF4↑+30CO↑ 蒸馏
【解析】
由流程可知,氟磷灰石经粉碎后与浓硫酸反应可以生成HF气体,气体以液化后与NaCl混合搅拌、溶解得到混合液;氟磷灰石与焦炭和石英砂在高温下反应可以得到白磷,白磷与氯气在点燃的条件下反应得到固体B,B为五氯化磷;B与混合液反应可以生成HCl,反应后的混合液在油浴中加热可以得到六氟磷酸钠粗品;粗品经提纯得到精品。
(1)固体反应物的颗粒越小,其反应的接触面积越大,化学反应速率越快。氟磷灰石粉碎的目的是:增大反应物的接触面积,加快反应速率。
(2)HF液化时产生的二聚物(HF)2能发生微弱的电离,与NaCl反应生成NaHF2,该二聚物的电离方程式为(HF)2H++![]() 或 2HFH++
或 2HFH++![]() 。
。
(3)为避免废水NaH2PO4的污染,常在其中加入石灰,将磷元素全部转化成磷酸钙,进行回收利用。已知常温下Ksp[Ca3(PO4)2]=1.96×10-29,当处理后的废水c(Ca2+)=1.0×10-5 mol/L时,则溶液中c(![]() )=
)=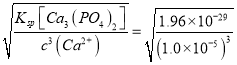 mol/L =1.4×10-7mol/L。
mol/L =1.4×10-7mol/L。
(4)HF 极易溶于水,HF在反应中可能是过量的,操作③油浴加热目的是除去残留的氟化氢。
(5)反应①中除生成白磷(P4)外,还产生SiF4和一种还原性气体,该气体是焦炭的氧化产物CO,该反应的化学方程式:4Ca5(PO4)3F+21SiO2+30C![]() 20CaSiO3+3P4+SiF4↑+30CO↑。
20CaSiO3+3P4+SiF4↑+30CO↑。
(6) 六氟磷酸钠(NaPF6)极易溶于水,可溶于乙醇、丙酮等有机溶剂。提纯六氟磷酸钠粗品时,为减少产品的损失,且考虑到产品易与溶剂分离,选择沸点较低的醇作溶剂。将六氟磷酸钠粗品(杂质主要是微量铁盐)溶于一定量乙醇中,加入适量5%的NaOH甲醇溶液,使溶液保持碱性,离心将不溶杂质除去。通过蒸馏将溶剂回收,减压条件下结晶,得到NaPF6·H2O,干燥得到无水盐。


科目:高中化学 来源: 题型:
【题目】三室式电渗析法处理含乳酸(HA表示乳酸分子,A-表示乳酸根离子)废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,下列说法正确的是( )
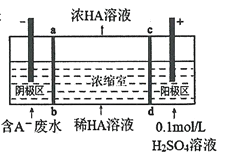
A.阴极区电极反应式为4OH--4e-=2H2O+O2↑
B.交换膜cd为阳离子交换膜,H+从阳极区通过阳离子交换膜进入浓缩室
C.通电一段时间后浓缩室水的量减少,导致乳酸溶液增大
D.当电路中通过1mol电子的电量时,两极一定共产生11.2L(标准状况下)气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿司匹林(Aspirin,乙酰水杨酸)具有解热止痛,抑制血小板凝聚,防止血栓形成的功效,是家庭中常备药品。水杨酸与乙酸酐反应制取阿司匹林的原理如图:
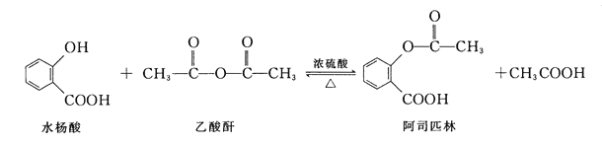
下列有关说法错误的是
A.水杨酸分子中所有原子可能共面
B.水杨酸的同分异构体中,属于苯环上二元取代物的还有5种(不考虑过氧键)
C.乙酰水杨酸在一定条件下能发生加成、水解、酯化等反应
D.分离乙酰水杨酸和乙酸可以加入饱和Na2CO3溶液后分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硫酸渣(主要含Fe2O3、FeO,杂质为Al2O3和SiO2等)为原料制备铁黄(FeOOH)的一种工艺流程如下:
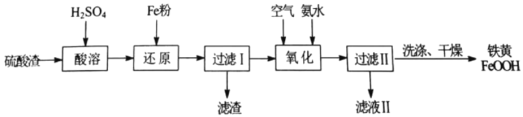
(1)“酸溶”时加快溶解的方法可以是________。(写出一种)
(2)“还原”过程中主要反应的离子方程式为________。
(3)“氧化”过程中,生成FeOOH的离子方程式为________。
(4)“过滤Ⅱ”所得铁黄在洗涤过程中,检验铁黄表面已洗涤干净的操作是________。
(5)实验测得反应溶液的![]() 、温度对铁黄产率的影响如图1、图2所示。
、温度对铁黄产率的影响如图1、图2所示。
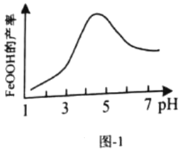
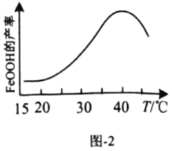
①反应温度宜选择________;
②氧化时应控制pH的合理范围是4.5左右,pH过小或过大均会导致铁黄产率较低,其可能原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A.BrCH2CHBrCH2Br的名称为三溴丙烷
B.甘氨酸和丙氨酸混合物脱水成肽,最多可生成4种二肽
C.萘环(![]() )上的一个H 原子被—C4H9 取代后的产物共有32种
)上的一个H 原子被—C4H9 取代后的产物共有32种
D.C3H6 和C4H8 不一定是同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语书写正确的是( )
A.金属发生电化学腐蚀的正极反应式:M-ne-=Mn+
B.家用小苏打溶于水后的电离:NaHCO3=Na++H++CO![]()
C.氯化铁溶液制备氢氧化铁胶体:Fe3++3H2O=Fe(OH)3↓+H+
D.用碳酸钠溶液处理锅炉水垢中的硫酸钙:CaSO4(s)+CO![]() (aq)CaCO3(s)+SO
(aq)CaCO3(s)+SO![]() (aq)
(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近科学家研发了“全氢电池”,其工作原理如图所示。下列说法不正确的是( )

A.吸附层b为电池的正极
B.“全氢电池”的总反应为:H++OH-=H2O
C.NaClO4的作用是传导离子并参与电极反应
D.Na+在装置中从左侧透过阳离子交换膜向右侧移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验室废液含![]() 等离子,现通过如下流程变废为宝制备
等离子,现通过如下流程变废为宝制备![]() 。
。
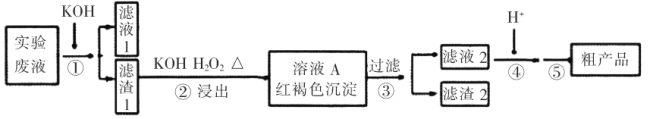
已知:(a)![]()
![]() (黄色)
(黄色)
(b)金属离子形成氢氧化物沉淀的pH范围如表。
金属离子 | pH | |
沉淀 | 沉淀 | |
Fe3+ | 2.7 | 3.7 |
Cr3+ | 4.9 | 6.8 |
请回答:
(1)如在试管中加入少量(NH4)2Cr2O7固体,滴加足量浓KOH溶液,振荡、微热,观察到的主要现象是:_________________。
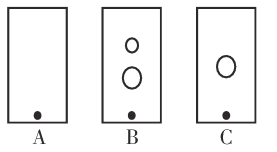
(2)某同学采用纸层析法判断步骤①加入KOH的量是否合适。在加入一定量KOH溶液后,用毛细管取样、点样、薄层色谱展开、氨熏后的点如图所示。加入KOH最适合的实验编号是(上图ABC中选择,实验顺序已乱)_________________,C的斑点颜色为_________________。
(3)步骤②含Cr物质发生的主要反应的离子方程式为_________________。
(4)在下列装置中,步骤②应选用实验装置是_________________。(填标号)
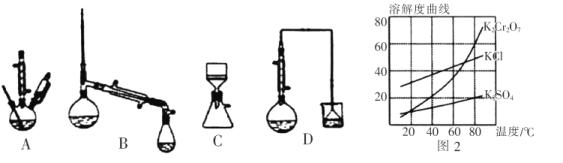
(5)部分物质的溶解度曲线如图2,步骤⑤可能用到下列部分操作:a.蒸发至出现大量晶体,停止加热;b.冷却至室温;c.蒸发至溶液出现晶膜,停止加热;d.洗涤;e.趁热过滤;f.抽滤。请选择合适操作的正确顺序_________________。
(6)步骤⑤中合适的洗涤剂是_________________(“无水乙醇”、“乙醇-水混合液”、“热水”、“冰水”),粗产品进一步提纯的方法是_________________。
(7)取mg粗产品配成250mL溶液,取25.00mL于锥形瓶中,用cmol.L-1的![]() 标准溶液滴定(杂质不反应),消耗标准
标准溶液滴定(杂质不反应),消耗标准![]() 溶液VmL,则该粗产品中
溶液VmL,则该粗产品中![]() 的纯度为_________________。(
的纯度为_________________。(![]() 的式量:294)
的式量:294)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次递增,a、b、c、d、e、f是由这些元素组成的化合物,a的一种重要用途为清洁能源,d是淡黄色粉末,m为元素Y的单质,通常为无色无味的气体。上述物质的转化关系如图所示。下列说法错误的是( )
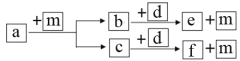
A.简单离子半径:Z<Y
B.阴离子的还原性:Y>W
C.简单气态氢化物的热稳定性:Y>X
D.W2Y2中含有非极性键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com