
(2009广东佛山质检,26)在阿富汗战争和伊拉克战争中美军士兵佩带的头盔、防弹背心和刚性前后防护板能够有效防御子弹和炮弹碎片,它们在战争中保住了许多美军士兵的生命。新型纤维不久将有望取代使用了数十年的凯夫拉纤维,成为未来防弹装备的主要制造材料。M5纤维是近年来开发出的一种超高性能纤维,它比现有的防爆破材料轻35%,下面是M5纤维的合成路线(部分反应未注明条件):

已知:当反应条件为光照且与X2反应时,通常是X2与烷或苯环侧链烃基上的H原子发生的取代反应,而当反应条件为催化剂存在且与X2反应时,通常为苯环上的H原子直接被取代。根据上述合成M5纤维的过程,回答下列问题:
(1)合成M5的单体G的结构简式为_______________,F的含氧官能团的名称有___________。
(2)在①~⑦的反应中,不属于取代反应的是___________,②的反应条件是______________。
(3)生成A的同时可能生成的A的同分异构体为_________________________________。
(4)1 mol的C和足量新制的氢氧化铜悬浊液反应可以生成___________mol砖红色沉淀。
(5)1 mol的F和Na2CO3溶液反应最多消耗Na2CO3___________mol。
科目:高中化学 来源: 题型:阅读理解
 (2009?广东)铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂.
(2009?广东)铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂.
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
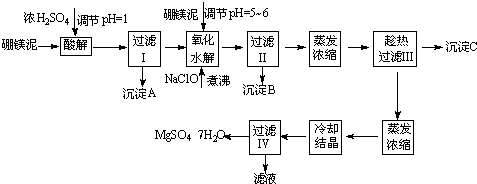
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
| pH值 | 5.2 | 3.2 | 9.7 | 10.4 | 11.2 |
| 温度/℃ | 10 | 30 | 40 | 50 | 60 |
| CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 | 0.19 |
| MgSO4?7H2O | 30.9 | 35.5 | 40.8 | 45.6 | / |
查看答案和解析>>
科目:高中化学 来源: 题型:
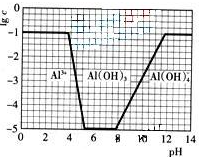 (2009?广东)超细氧化铝是一种重要的功能陶瓷原料.
(2009?广东)超细氧化铝是一种重要的功能陶瓷原料. Al2O3+3H2O↑+2CO2↑+2NH3↑
Al2O3+3H2O↑+2CO2↑+2NH3↑ Al2O3+3H2O↑+2CO2↑+2NH3↑
Al2O3+3H2O↑+2CO2↑+2NH3↑查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com