
| A. | 常温下,2.24LCH4中含有0.4NA个共价键 | |
| B. | 100mL1mol•L-1NaAlO2溶液中含有0.1NA个AlO2- | |
| C. | 常温常压下,5.6gFe与足量稀硝酸反应,转移电子0.2NA个电子 | |
| D. | 标准状况下,1.12L1H2和0.2g2H2均含有0.1NA个质子 |
分析 A、常温常压下,气体摩尔体积大于22.4L/mol;
B、偏铝酸根为弱酸根,在溶液中会水解;
C、求出铁的物质的量,然后根据铁和足量硝酸反应变为+3价来分析;
D、求出1H2和2H2的物质的量,然后根据1H2和2H2中均含2个质子来分析.
解答 解:A、常温常压下,气体摩尔体积大于22.4L/mol,故2.24L甲烷的物质的量小于0.1mol,则含有的共价键小于0.4NA个,故A错误;
B、偏铝酸根为弱酸根,在溶液中会水解,故溶液中的偏铝酸根个数小于0.1NA个,故B错误;
C、5.6g铁的物质的量为0.1mol,而铁和足量硝酸反应变为+3价,故0.1mol铁转移0.3NA个电子,故C错误;
D、标况下1.12L1H2的物质的量为0.05mol,0.2g2H2的物质的量也为0.05mol,而1H2和2H2中均含2个质子,故0.05mol1H2和2H2中含0.1mol质子即0.1NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,根据物质的结构并利用公式来运算是解题的关键,难度不大.


 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:填空题
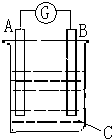 请根据图所示回答:甲装置是由铜、锌和稀硫酸组成的原电池,
请根据图所示回答:甲装置是由铜、锌和稀硫酸组成的原电池,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 六种元素周期表中的位置如图,其中只有一种不是短周期元素,只有一种是金属元素,下列说法正确的是( )
六种元素周期表中的位置如图,其中只有一种不是短周期元素,只有一种是金属元素,下列说法正确的是( )| A. | 简单离子半径大小:Q>Y>X | |
| B. | 最简单气态氢化物的沸点高低:Y>Z | |
| C. | Q的最高价氧化物可与X的氢化物直接反应 | |
| D. | X与Y既可存在于同一共价化合物中,也可存在于同一离子化合物中 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
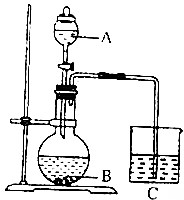 某化学小组设计如图装置完成一组实验;
某化学小组设计如图装置完成一组实验;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯中少量的苯酚可先加适量的浓溴水,使之生成三溴苯酚,再过滤除去 | |
| B. | 将苯酚晶体放入少量水中,加热时全部溶解,冷却后溶液仍澄清透明 | |
| C. | 苯酚的酸性很弱,不能使指示剂变色,但可以与NaCHO3反应放出CO2 | |
| D. | 苯酚有毒,但其稀溶液可直接用作防腐剂和消毒剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
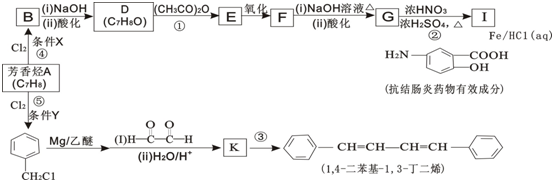
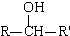 (R、R′表示烃基)
(R、R′表示烃基)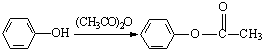
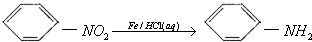
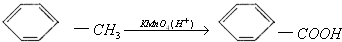
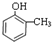
 .
.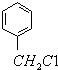 有氯原子的方法是将少量样品与NaOH溶液在试管中混合共热,充分反应并冷却后,向溶液中加稀HNO3酸化,再滴加AgNO3溶液,若有白色沉淀,则证明有氯元素.
有氯原子的方法是将少量样品与NaOH溶液在试管中混合共热,充分反应并冷却后,向溶液中加稀HNO3酸化,再滴加AgNO3溶液,若有白色沉淀,则证明有氯元素.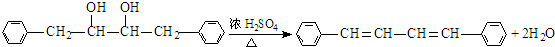 .
.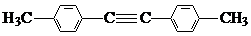
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子最外层电子数为2的元素一定处于周期表ⅡA族 | |
| B. | 主族元素X、Y能形成XY2型化合物,则X与Y的原子序数之差可能为2或5 | |
| C. | 氯化氢的沸点比氟化氢的沸点高 | |
| D. | 第三周元素的离子半径从左到右逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种 | B. | 4种 | C. | 5 种 | D. | 6种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com