
(10分)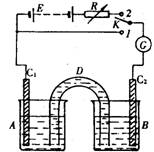 装置如右图:D是允许通过离子的盐桥,E是48V稳压电源,R是可变电阻,K是开关,G是灵敏电流计,C1、C2是碳棒,A、B是烧杯。
装置如右图:D是允许通过离子的盐桥,E是48V稳压电源,R是可变电阻,K是开关,G是灵敏电流计,C1、C2是碳棒,A、B是烧杯。
1.已知AsO43-+2I-+2H+![]() AsO33-+I2+H2O是可逆反应。若A中盛KI-I2溶液,B中盛Na3AsO4和Na3AO3溶液,则当K接1,并向B中滴加浓盐酸时发现G中的指针发生偏转;改向B中滴加40%的NaOH溶液时,G中的指针则向反方向偏转。
AsO33-+I2+H2O是可逆反应。若A中盛KI-I2溶液,B中盛Na3AsO4和Na3AO3溶液,则当K接1,并向B中滴加浓盐酸时发现G中的指针发生偏转;改向B中滴加40%的NaOH溶液时,G中的指针则向反方向偏转。
(1)两次操作过程中指针偏转的原因是
(2)指针偏转方向相反的原因是
(3)加盐酸时C1上发生的反应是
(4)加NaOH溶液时C1上发生的反应是
2.当 A中盛适量的1mol/L Na2SO4溶液,B中盛40mL适量浓度的KI-KHCO3溶液,且K接2时,可用该装置来测定砷的含量。其操作如下:称取5.00g含砷样品,溶解后加入还原剂,使砷全部转化为HAsO32-,除去过量的还原剂后再转移到250mL容量瓶中配成250mL溶液,用移液管从中取出10mL加入B中,边搅拌边电解,电解生成的 I2可将HAsO32-快速、定量地氧化为HAsO42-,以2mA的电流电解241s便可使反应进行完全。
(1)反应到达终点时宜用 来指示;
(2)假设电能没有损失,试求样品中As2O5的质量分数。
科目:高中化学 来源: 题型:
(08年江苏卷)(10分)金矿开采、冶炼和电镀工业会产生大量含氰化合物的污水,其中含氰化合物以HCN、CN -和金属离子的配离子M(CN)nm-的形式存在于水中。测定污水中含氰化合物含量的实验步骤如下:
①水样预处理:水样中加入磷酸和EDTA,在pH<2的条件下加热蒸馏,蒸出所有的HCN,并用NaOH溶液吸收。
②滴定:将吸收液调节至pH>11,以试银灵作指示剂,用AgNO3标准溶液滴定
 Ag++2CN - == [Ag(CN)2] -
Ag++2CN - == [Ag(CN)2] -
终点时,溶液由黄色变成橙红色。
根据以上知识回答下列问题:
⑴水样预处理的目的是 。
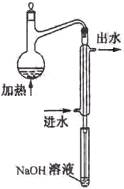
⑵水样预处理的装置如右图,细导管插入吸收液中是为了 ____
⑶蒸馏瓶比吸收液面要高出很多,其目的是 。
⑷如果用盐酸代替磷酸进行预处理,实验结果将 (填“偏高”、“无影响”或“偏低”)。
⑸准确移取某工厂污水100mL,经处理后用浓度为0.01000mol?L-1的硝酸银标准溶液滴定,终点时消耗了21.00mL。此水样中含氰化合物的含量为 mg?L-1的(以计,计算结果保留一位小数)。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年广东省东莞市第七高级中学高二下学期期中考试化学试卷(带解析) 题型:实验题
Ⅰ、下列实验操作不正确的是 ;
①用分液漏斗分离环己烷和苯的混合液体
②将10滴溴乙烷加入到1 mL 10%的烧碱溶液中,加热片刻后,冷却,先加过量的硝酸,再滴加2滴2%的硝酸银溶液,以检验水解生成的溴离子。
③分离苯和苯的同系物,可以采用蒸馏的方法。
④实验室制溴苯时选用的试剂可以是溴水、苯和铁屑
Ⅱ、为检验利用溴乙烷发生消去反应后生成的气体中是否含乙烯的装置如右图所示。回答: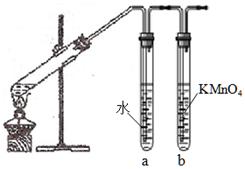
(1)溴乙烷发生消去反应的化学方程式为: ;
(2)试管a的作用是 ;
(3)若省去试管a,试管b中试剂为 。
查看答案和解析>>
科目:高中化学 来源:2008年普通高等学校招生统一考试化学试题(江苏卷) 题型:实验题
(10分)金矿开采、冶炼和电镀工业会产生大量含氰化合物的污水,其中含氰化合物以HCN、CN -和金属离子的配离子M(CN)nm-的形式存在于水中。测定污水中含氰化合物含量的实验步骤如下:
①水样预处理:水样中加入磷酸和EDTA,在pH<2的条件下加热蒸馏,蒸出所有的HCN,并用NaOH溶液吸收。
②滴定:将吸收液调节至pH>11,以试银灵作指示剂,用AgNO3标准溶液滴定
Ag++2CN - ="=" [Ag(CN)2] -
终点时,溶液由黄色变成橙红色。
根据以上知识回答下列问题:
(1)水样预处理的目的是 。
(2)水样预处理的装置如右图,细导管插入吸收液中是为了 。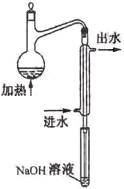
(3)蒸馏瓶比吸收液面要高出很多,其目的是 。
(4)如果用盐酸代替磷酸进行预处理,实验结果将 (填“偏高”、“无影响”或“偏低”)。
(5)准确移取某工厂污水100mL,经处理后用浓度为0.01000mol·L-1的硝酸银标准溶液滴定,终点时消耗了21.00mL。此水样中含氰化合物的含量为 mg·L-1(以CN-计,计算结果保留一位小数)。
查看答案和解析>>
科目:高中化学 来源:2010年福建省高三模拟考试(理综)化学部分 题型:填空题
(16分)应用化学反应需要研究化学反应的条件、限度和速率。
(1)已知反应:Br2+2Fe2+=2Br-+2Fe3+ ,向10 mL 0.1 mol·L-1的FeBr2溶液中通入0.001 mol Cl2,反应后,溶液中除含有Cl-外,还一定有 (填序号)。
①含Fe2+,不含Fe3+② 含Fe3+,不含Br-③ 含Fe3+,还含有Br-
(2)773 K、固定体积的容器中,反应CO(g)+2H2(g) CH3OH(g)过程中能量变化如下图。曲线Ⅱ表示使用催化剂时的能量变化。若投入a
mol CO、2a mol H2,平衡时能生成0.1a mol CH3OH,反应就具工业应用价值。
CH3OH(g)过程中能量变化如下图。曲线Ⅱ表示使用催化剂时的能量变化。若投入a
mol CO、2a mol H2,平衡时能生成0.1a mol CH3OH,反应就具工业应用价值。
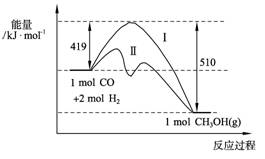
①若按上述投料比使该反应具有工业应用价值,CO的平衡转化率最小为 ;
②在容器容积不变的前提下,欲提高H2的转化率,可采取的措施(答两项即可) 、 ;
③下列与催化剂有关的说法中,正确的是 (填字母序号)。
a. 使用催化剂,使反应CO(g)+2H2(g) CH3OH(g) ΔH>-91
kJ·mol-1
CH3OH(g) ΔH>-91
kJ·mol-1
b. 使用催化剂, 能够提高反应物转化率
c. 使用催化剂,不能改变反应的平衡常数K
(3)高铁酸盐在能源环保领域有广泛用途。我国学者提出用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的方案,装置如右图所示。
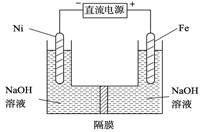
① Ni作 (填“阴”或“阳”) 极;
②Ni电极的电极反应式为: 。
(4)氧化还原反应中实际上包含氧化和还原两个过程。下面是HNO3发生的一个还原过程的反应式:NO-3+4H++3e-→NO+2H2O
①KMnO4、HCl、Fe(NO3)2、CuO、KI五种物质中的 (填化学式)能使上述还原过程发生。
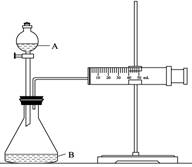
②欲用下图装置通过测定气体生成量测算硝酸被还原的速率,当反应物的浓度、用量及其他影响速率的条件确定之后,可以通过测定 推(计)算反应速率。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com