
| ��Ŀ | H2 | N2 | NH3 |
| ��ʼʱ | 5 mol��L��1 | 3 mol��L��1 | 0 |
| 2 sĩ | 2 mol��L��1 | | |

 2NH3(g)�ͱ������ݣ������v(H2)��1.5 mol��L��1��s��1���ﵽƽ��ʱ�����ʵ�Ũ�ȷֱ�Ϊn(H2)��2 mol��L��1��n(N2)��2 mol��L��1��n(NH3)��2 mol��L��1���������ƽ�ⳣ��Ϊ0.25��
2NH3(g)�ͱ������ݣ������v(H2)��1.5 mol��L��1��s��1���ﵽƽ��ʱ�����ʵ�Ũ�ȷֱ�Ϊn(H2)��2 mol��L��1��n(N2)��2 mol��L��1��n(NH3)��2 mol��L��1���������ƽ�ⳣ��Ϊ0.25��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ͬ�����£�2molSO2��1molO2�����е�����С��2molSO3�����е����� |
| B����2molSO2��g����1molO2��g������һ�ܱ������г�ַ�Ӧ�ų�����ΪQkJ |
| C������ѹǿ�������¶ȣ���ƽ�ⶼ���淴Ӧ�����ƶ� |
| D���罫һ����SO2��g����O2��g������ij�ܱ������г�ַ�Ӧ�����QkJ����˹�������2molSO2��g�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ | B����ѹ | C����ѹ | D������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
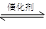 2CO2��N2
2CO2��N2| ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/ mol��L-1 | 1.00��10-3 | 4.50��10-4 | 2.50��10-4 | 1.50��10-4 | 1.00��10-4 | 1.00��10-4 |
| c(CO)/ mol��L-1 | 3.60��10-3 | 3.05��10-3 | 2.85��10-3 | 2.75��10-3 | 2.70��10-3 | 2.70��10-3 |
 0�����>������<������=������
0����д��>������<������=������| ʵ���� | T/�� | NO��ʼŨ�� mol��L-1 | CO��ʼŨ�� mol��L-1 | �����ıȱ���� �O��g-1 |
| �� | 280 | 1.2��10-3 | 5.8��10-3 | 82 |
| �� | | | 5.8��10-3 | 124 |
| �� | 350 | 1.2��10-3 | | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2N2O5(g)����֪�÷�Ӧ��ƽ�ⳣ����K300 ����K350 ������n(NO2)(��λ��mol)��ʱ��仯���±���
2N2O5(g)����֪�÷�Ӧ��ƽ�ⳣ����K300 ����K350 ������n(NO2)(��λ��mol)��ʱ��仯���±���| ʱ��(s) | 0 | 500 | 1000 | 1500 |
| t1�� | 20 | 13.96 | 10.08 | 10.08 |
| t2�� | 20 | a | b | c |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����֪��G=��H-T��S, ��G ��0��Ӧ�Է����У�2CO(g)+2NO(g) ��N2(g)+2CO2(g)���¶�Ϊ298��ʱ���Է����У������ġ�H��0 |
| B��0.1 mol��L-1Na2CO3��Һ������ˮϡ�ͣ�CO32����ˮ��̶ȱ����Һ��pH�������� |
| C����⾫��ͭ�����У����������ļ�����������������������һ����� |
D��C(s)+CO2(g)  2CO(g) �SH��0��������������ʱ���{�¶ȣ�CO2�ķ�Ӧ���ʺ�ƽ��ת���ʾ����� 2CO(g) �SH��0��������������ʱ���{�¶ȣ�CO2�ķ�Ӧ���ʺ�ƽ��ת���ʾ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������


 ����ش��������⣺
����ش��������⣺
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2NO2(g)����H��0����һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�
2NO2(g)����H��0����һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�| t/s c/(mol��L��1)���� | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)/(mol��L��1) | 0.100 | a | 0.5b | 0.4b | | |
| c(NO2)/(mol��L��1) | 0 | 0.060 | b | c1 | c2 | c3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CH3OH(g)���ݻ�Ϊ1L�����ܱ������зֱ����1molCO��2molH2��ʵ���ü״������ʵ������¶ȡ�ʱ��Ĺ�ϵ������ͼ��ʾ���������Ӧ�ġ�H_______0�����������������=�������жϵ�������______��
CH3OH(g)���ݻ�Ϊ1L�����ܱ������зֱ����1molCO��2molH2��ʵ���ü״������ʵ������¶ȡ�ʱ��Ĺ�ϵ������ͼ��ʾ���������Ӧ�ġ�H_______0�����������������=�������жϵ�������______��
 CH3OH+H2O��
CH3OH+H2O��

 CO(g)+2H2(g)�����ݻ�Ϊ2.0L���ܱ������г���0. 60 molCH3OH(g)����ϵѹǿΪP1����һ�������´ﵽƽ��ʱ����ϵѹǿΪP2����P2/P1 =2.2�����������CH3OH ��ƽ��ת����Ϊ______ ��
CO(g)+2H2(g)�����ݻ�Ϊ2.0L���ܱ������г���0. 60 molCH3OH(g)����ϵѹǿΪP1����һ�������´ﵽƽ��ʱ����ϵѹǿΪP2����P2/P1 =2.2�����������CH3OH ��ƽ��ת����Ϊ______ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com