
 CO��H2�Ļ�������׳ƺϳ�������һ����Ҫ�Ĺ�ҵԭ������������һ���������Ʊ��״��������ѵȶ����л����ҵ��������Ȼ������Ҫ�ɷ�ΪCH4����ˮ���и��������Ʊ��ϳ�����
CO��H2�Ļ�������׳ƺϳ�������һ����Ҫ�Ĺ�ҵԭ������������һ���������Ʊ��״��������ѵȶ����л����ҵ��������Ȼ������Ҫ�ɷ�ΪCH4����ˮ���и��������Ʊ��ϳ�����| ʱ��/min ���� Ũ�� |
0 | 1 | 2 | 3 | 4 |
| CH4 | 0.2mol?L-1 | 0.13mol?L-1 | 0.1mol?L-1 | 0.1mol?L-1 | 0.09mol?L-1 |
| H2 | 0mol?L-1 | 0.2mol?L-1 | 0.3mol?L-1 | 0.3mol?L-1 | 0.33mol?L-1 |
| 1 |
| 2 |
| 1 |
| 2 |
| 8.96L |
| 22.4L/mol |
| 0.4mol��4 |
| 8 |


 ���źþ���Ԫ����ĩ��ϵ�д�
���źþ���Ԫ����ĩ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
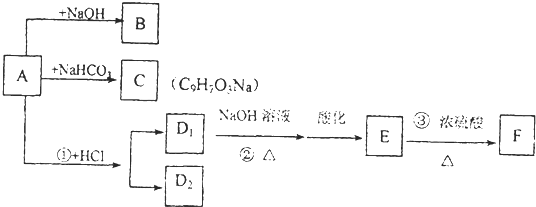
| A������ˮ�ķ�Ӧ��Na+2H2O=Na++2OH-+H2�� |
| B��������NaHSO4��Ba��OH��2��Һ��Ӧ��Ba2++2OH-+2H++SO42-�TBaSO4��+2H2O |
| C������þ��Һ������������Һ��Ӧ��SO42-+Ba2+=BaSO4�� |
| D��̼������ڴ����� CaCO3+2H+=Ca2++H2O+CO2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na+��NH4+��Fe2+��NO3-��ϡ���ᣩ |
| B��Al3+��K+��HCO3-��NO3-��NaOH��Һ�� |
| C��NH4+��Ag+��K+��NO3-��NaOH��Һ�� |
| D��Na+��K+��AlO2-��SiO32-��ϡ���ᣩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��PCl3��PCl5 |
| B��MnO2��Mn2+ |
| C��SO2��SO2-3 |
| D��Fe��Fe2O3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
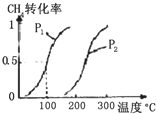 �״�����Ϊ21���͵�����ȼ�ϣ���ҵ����CH4��H2OΪԭ��ͨ�����з�Ӧ�ٺ͢ڣ����Ʊ��״���
�״�����Ϊ21���͵�����ȼ�ϣ���ҵ����CH4��H2OΪԭ��ͨ�����з�Ӧ�ٺ͢ڣ����Ʊ��״���| ʵ���� | T����C�� | n��CO��/n��H2�� | p��MPa�� | ||
| I | 150 |
|
0.1 | ||
| II | 5 | ||||
| III | 350 | 5 |
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com