
【题目】增大压强对下列反应的速率无影响的是 ( )
A.CO2(g) + Ca(OH)2 = CaCO3↓ + H2O B.H2 + I2 ![]() 2HI
2HI
C.NaCl +AgNO3 = AgCl↓ + NaNO3 D.N2 +3H2 ![]() 2NH3
2NH3
【答案】C
【解析】
试题分析:增大压强只对有气体参加或者有气体生成的化学反应的速率才有影响,A. CO2(g) + Ca(OH)2 = CaCO3↓ + H2O ,有气体参加反应,所以增大压强对化学反应速率有加快的作用,A错误;B.H2 + I2 ![]() 2HI,有气体参加反应,所以增大压强可以加快化学反应速率,B错误;C.反应 NaCl +AgNO3 = AgCl↓ + NaNO3中,既没有气体生成,也没有气体参加反应,所以增大压强对化学反应速率没有影响,C正确;D.N2 +3H2
2HI,有气体参加反应,所以增大压强可以加快化学反应速率,B错误;C.反应 NaCl +AgNO3 = AgCl↓ + NaNO3中,既没有气体生成,也没有气体参加反应,所以增大压强对化学反应速率没有影响,C正确;D.N2 +3H2 ![]() 2NH3是一个有气体参加和生成的化学反应,所以增大压强对化学反应速率起到加快的作用,D错误,答案选C。
2NH3是一个有气体参加和生成的化学反应,所以增大压强对化学反应速率起到加快的作用,D错误,答案选C。


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:
【题目】许多有机化合物具有酸碱性.
完成下列填空:
(1)苯酚、苯甲酸、碳酸的酸性由强到弱的顺序为 .
(2)常常利用物质的酸碱性分离混合物.某一混合物含苯酚、苯甲醇、苯甲酸和苯胺四种物质,其分离方案如下图.
已知:苯甲醇、苯甲酸、苯胺微溶于水,且苯胺( ![]() )具有碱性.
)具有碱性.
A、B、C分别是:A , B , C
上述方案中,若首先仅仅将苯甲酸与其他三种物质分开,则应加入 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2与O2发生反应的过程用模型图示如下(“﹣”表示化学键):下列说法不正确的是( ) 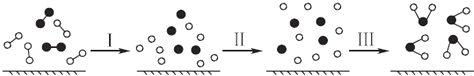
A.过程Ⅰ是吸热过程
B.过程Ⅲ一定是放热过程
C.该反应过程所有旧化学键都断裂,且形成了新化学键
D.该反应的能量转化形式只能以热能的形式进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2+O2![]() 2H2O。
2H2O。
(1)该反应1g氢气完全燃烧放出热量121.6kJ,其中断裂1molH-H键吸收436kJ,断裂1molO=O键吸收496kJ,那么形成1molH-O键放出热量____________________。
(2)原电池是直接把化学能转化为电能的装置。
I.航天技术上使用的氢-氧燃料电池具有高能、轻便和不污染环境等优点。下图是氢-氧燃料电池的装置图。则:

①溶液中OH-移向________电极(填“a”或“b”)。
②b电极附近pH_____________。(填增大、减小或不变)
③如把H2改为甲烷,则电极反应式为:正极:____________________________,负极:________________________________。
II.将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g,试计算:产生氢气的体积___________________________________L。(标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学假说是科学发展的一种重要形式。有科学家提出: 利用空气中的二氧化碳与氢气反应后,使之变为可再生的燃料甲醇的设想。其设想的生产流程如图。下列说法正确的是

A. 上述流程中饱和碳酸钾溶液所起的作用是降低空气中的CO2 的溶解度
B. 上述流程中能体现“循环利用”的物质有碳酸氢钾溶液和高温水蒸气
C. 从合成塔中分离出甲醇的实验操作方法是分液
D. 通入高温水蒸气的作用是: 加快CO2的生成和逸出,以便及时提供给合成塔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的性质与应用关系的描述不正确的是()
A.氧化镁的熔点高,是优质的耐高温材料
B.金属钠着火,不可用泡沫灭火器灭火
C.氯气有强氧化性,可用氯气漂白干燥的有色布条
D.二氧化硫有漂白性,可用于漂白毛,丝,纸浆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度下,四种一元弱酸的电离平衡常数为:Ka(HCN)=6.2×10-10 mol/L、Ka(HF)=6.8×10-4 mol/L、Ka(CH3COOH)=1.8×10-5 mol/L、Ka(HNO2)=6.4×10-6 mol/L。物质的量浓度都为0.1 mol/L的下列溶液中,pH最小的是( )
A. HCN B. CH3COOH C. HF D. HNO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化碘(ICl3)在药物合成中用途非常广泛,其熔点为33℃,沸点为73℃。实验室可用如图装置制取ICl3。

(1)仪器a的名称是___________________。
(2)制备氯气选用的药品为漂白粉固体(主要成分为CaClO2)和浓盐酸,相关反应的化学方程式为_______________________________________。
(3)装置B可用于除杂,也是安全瓶,能监测实验进行时装置C中是否发生堵塞,请写出发生堵塞时B中的现象:____________________________。
(4)试剂X为____________________________。
(5)氯气与单质碘需在温度稍低于70℃下反应,则装置D适宜的加热方式为___________________。
(6)欲测定上述实验制备ICl3样品中ICl3的纯度,准确称取ICl3样品10.0g于烧杯中,加入适量水和过量KI 晶体,充分反应生成I2(样品中杂质不反应)。写出反应的方程式_________________________;将所得溶液配置成100mL待测液,取25.00mL待测液,用2.0mol/L的Na2S2O3标准液滴定(I2+2S2O32- =2I-+ S4O62-),以淀粉溶液作指示剂,达到终点时的现象为______________________;重复滴定,实验数据记录如下:
滴定次数 | 待测液体积(mL) | Na2S2O3标准液体积/mL | |
滴定前读数(mL) | 滴定后读数(mL) | ||
1 | 25.00 | 0.50 | 20.40 |
2 | 25.00 | 4.00 | 24.10 |
3 | 25.00 | 4.20 | 26.70 |
该样品中ICl3的质量分数为____________________。(ICl3相对分子质量为233.5)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com