
����Ŀ��ij�о�С���û�ͭ��(��Ҫ�ɷ���CuFeS2������SΪ-2��)Ϊ��Ҫԭ����ͭ�����ܷ�ӦΪ��2CuFeS2+2SiO2+5O2��2Cu+2FeSiO3+4SO2����ʵ�ϸ÷�Ӧ�ǰ��������̷ֲ����еģ�
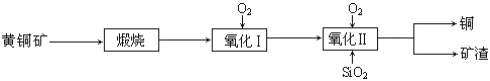
(1)�������ķ�Ӧ��Ҫ���������ɵ�����������һ������Ϊ��������������������跴Ӧ���ɿ�������������Ҫ�ɷ���(�ѧʽ)_____________________��
(2)�ݱ�������һ��ϸ�������������¿��Խ���ͭ�������������Σ���Ӧ����������Һ�з����ġ��÷�Ӧ�Ļ�ѧ����ʽΪ____________________��
(3)�ҹ�ѧ���о����֣��Ծ�CuFeS2��Ϊԭ���ڷ���¯����O2(����)��Ӧ����������ȴ���ܽ⡢�������ᾧ���õ�CuSO4��5H2O�������ɱ��ܹ��������ࡣ�й�ʵ�������±���
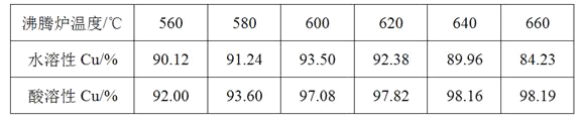
��CuFeS2��O2��Ӧ�Ļ�ѧ����ʽΪ______________________��
��ʵ�����������з���¯�¶�Ϊ600��620 ����������¶ȵķ�����_______________��
�����¶ȸ���600��620 ��ʱ����������ˮ����ͭ�½���ԭ����____________��
����������ȴ��ij�����ʵ�����������Ҫ��_________����֪����Һ�У�Cu2+��ʼ�����ͳ�����ȫ��pH�ֱ�Ϊ4.7��6.7��Fe3+��ʼ�����ͳ�����ȫ��pH�ֱ�Ϊ1.1��3.2������Ƶõ�����ͭ��Һ�к���������Fe3+����д����ȥ��Һ��Fe3+��ʵ��������裺_______________��
���𰸡�FeSiO3 4CuFeS2+2H2SO4+17O2![]() 4CuSO4+2Fe2(SO4)3+2H2O 4CuFeS2+15O2��4CuSO4+2Fe2O3+4SO2 ���Ƽ���CuFeS2���ٶ�(��CuFeS2��O2��Ӧ����) CuSO4���ȷֽ� ���� ����CuO[��Cu(OH)2��CuCO3]��ĩ����ֽ��裬������Һ��pHԼΪ3.2��������У����ˣ���(����)ϡ�����ữ
4CuSO4+2Fe2(SO4)3+2H2O 4CuFeS2+15O2��4CuSO4+2Fe2O3+4SO2 ���Ƽ���CuFeS2���ٶ�(��CuFeS2��O2��Ӧ����) CuSO4���ȷֽ� ���� ����CuO[��Cu(OH)2��CuCO3]��ĩ����ֽ��裬������Һ��pHԼΪ3.2��������У����ˣ���(����)ϡ�����ữ
��������
��1������2CuFeS2+2SiO2+5O2��2Cu+2FeSiO3+4SO2���ɵÿ���ΪFeSiO3��
�ʴ�Ϊ��FeSiO3��
��2���������֪��CuFeS2��������Һ����������һ��ϸ�������������ɵ�������������ͭ������������ѧ����ʽΪ4CuFeS2+2H2SO4+17O2![]() 4CuSO4+2Fe2(SO4)3+2H2O��
4CuSO4+2Fe2(SO4)3+2H2O��
�ʴ�Ϊ��4CuFeS2+2H2SO4+17O2![]() 4CuSO4+2Fe2(SO4)3+2H2O��
4CuSO4+2Fe2(SO4)3+2H2O��
��3���پ�CuFeS2��Ϊԭ���ڷ���¯����O2����������Ӧ�����յ�CuSO4��5H2O��˵����Ԫ�صĴ�����ʽ������������ˮ�ܽ�ɹ��˳�ȥ������CuFeS2��O2��Ӧ�Ļ�ѧ����ʽΪ4CuFeS2+15O2��4CuSO4+2Fe2O3+4SO2��
�ʴ�Ϊ��4CuFeS2+15O2��4CuSO4+2Fe2O3+4SO2��
����ΪCuFeS2��O2��Ӧ���ȣ����������������п��Ƽ���CuFeS2���ٶȣ������¶ȣ�
�ʴ�Ϊ�����Ƽ���CuFeS2���ٶ�(��CuFeS2��O2��Ӧ����)��
��ˮ����ͭ������ΪCuSO45H2O��������ͭ������ΪCuO���¶Ƚϸ�ʱ��CuSO45H2O�ɷֽ�����CuO������600������ʱˮ����ͭ�����ﺬ�����٣�
�ʴ�Ϊ��CuSO4���ȷֽ⣻
���������г�����ͭ�����������������������ˮ��������ȴ��ij�����ʵ�����������Ҫ�ǹ��ˣ���ȥ�����Ӷ�����ȥͭ���ӣ�������Һ��pHֵ��3.2��4.7֮�䣬ʹ��������ȫ��������ͭ���Ӳ����������Ծ�������Ǽ���CuO[��Cu(OH)2��CuCO3]��ĩ����ֽ��裬������Һ��pHԼΪ3.2��������У����ˣ��ã�������ϡ�����ữ��
�ʴ�Ϊ������CuO[��Cu(OH)2��CuCO3]��ĩ����ֽ��裬������Һ��pHԼΪ3.2��������У����ˣ���(����)ϡ�����ữ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ�����仯���������-������άͼ��

��1����д��άͼȱʧ������___�ͻ�ѧʽ��___��
��2��ijͬѧ���������Լ��о�FeCl3���ʣ�����������Ԥ�⣺
��Cl2 ��Fe ��NaOH ��H2SO4 ��AgNO3
����������Ͽ���FeCl3����___��������___������Ӧ������ţ���
�ӻ��ϼ۽Ƕȿ���Fe3+����___�ԣ�������___������Ӧ������ţ���
��3��ij������FeCl3��Һ��ʴ����ͭ�ľ�Ե������ӡˢ��·���仯ѧԭ��Ϊ���·�Ӧ��Cu+2FeCl3=CuCl2+2FeCl2
���õ����ű�ʾ����ת�ơ�___��
�ڷ�Ӧ��FeCl3��___����������___��
��д���÷�Ӧ�����ӷ���ʽ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����״���£��������NH3��CH4�������壬�����й�˵���������
A.����������Ŀ��ͬB.������ԭ�����ʵ���֮��Ϊ3��4
C.����֮��Ϊ16��17D.�ܶ�֮��Ϊ17��16
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡ100mL��Na2CO3��Na2SO4�����Һ����������Ba(OH)2��Һ100 mL��ǡ����ȫ��Ӧ�����ˡ������õ�14.51g��ɫ��������Һ�����ù���ϡ���ᴦ�������������ٵ�4.66g����������ų������㣺
��1����ԭ���Һ��Na2SO4�����ʵ�����__________________
��2�������������ڱ�״���µ����Ϊ���٣�_________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ����ȷ����(����)
A. ��NaHCO3��Һ�м��������Ba(OH)2��Һ��2HCO3-��Ba2����2OH��===BaCO3����2H2O��CO32-
B. �����缫��ⱥ��ʳ��ˮ��2Cl����2H2O![]() 2OH����H2����Cl2��
2OH����H2����Cl2��
C. ��NaNO2��Һ�м�������KMnO4��Һ��2MnO4-��5NO2-��6H��===2Mn2����5NO3-��3H2O
D. ��Fe(NO3)3��Һ�м��������HI��Һ��2Fe3����2I��===2Fe2����I2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������X��Y��Z����Է���������ϵΪMr(X)<Mr(Y)��0��5Mr(Z)������˵����ȷ����
A. ԭ����Ŀ��ȵ��������壬����������Z
B. ͬ��ͬѹ�£�ͬ�������������壬�����ܶ���С����X
C. ��һ�������£��������������Ϊ2��24 L�������ǵ����ʵ���һ����Ϊ0.1 mol
D. ͬ���£������ͬ���������ֱ��2 g Y�����1 g Z���壬����ѹǿ��Ϊ2�U1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ�״���£�ag����A��bg����B�ķ�������ͬ��������йص�����˵���в���ȷ����
A.����A������B��Ħ������֮��Ϊ![]()
B.��ͬ״���£�ͬ���������A������B������֮��Ϊ![]()
C.������ͬ������A������B�ķ�����֮��Ϊ![]()
D.ͬ��ͬѹ�£�����A������B���ܶ�֮��Ϊ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ��H= ��1025kJ/mol������Ӧ����ʼ���ʵ�����ͬ�����й��ڸ÷�Ӧ��ʾ��ͼ����ȷ����( )
4NO(g)+6H2O(g) ��H= ��1025kJ/mol������Ӧ����ʼ���ʵ�����ͬ�����й��ڸ÷�Ӧ��ʾ��ͼ����ȷ����( )
A.  B.
B. 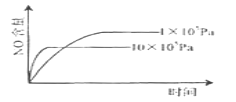
C.  D.
D. 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� 4 mol A ����� 2 mol B ������ 2 L �Ķ��������л�ϲ���һ�������·������·�Ӧ 2A��g����B��g��![]() 2C��g�� ��H<0 ���� 2 s���룩���� C ��Ũ��Ϊ 0. 6 mol��L-1 ���������м���˵����
2C��g�� ��H<0 ���� 2 s���룩���� C ��Ũ��Ϊ 0. 6 mol��L-1 ���������м���˵����
�� ������ A ��ʾ�ķ�Ӧ��ƽ������Ϊ 0.3 mol��L-1s-1
�� �ﵽƽ��״̬ʱ�������¶ȣ���û�ѧƽ�������ƶ���ͬʱ��ѧƽ�ⳣ��KҲ��С
�� 2 s ʱ���� A ��ת����Ϊ70��
�� �ﵽƽ��״̬ʱ������A���ʵ�����A��Bת���ʶ����
�ݵ�������Ũ������c(A)=2c(B)= c(C)ʱ���÷�Ӧ�ﵽ��ƽ��״̬
������ȷ���ǣ� ��
A. �٢� B. �٢� C. �ڢ� D. �ۢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com