
| A.浓硫酸、浓硝酸在加热条件下都能将木炭氧化为二氧化碳 |
| B.将氢氧化铁胶体与氯化铁溶液分别加热蒸干并灼烧,最终得到的物质成分不同 |
C.向NaClO溶液中通入足量SO2的离子方程式:ClO-+SO2+H2O=HClO+HSO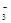 |
| D.铁粉与足量稀硝酸反应时,氧化剂与还原剂的物质的量之比为2∶3 |
科目:高中化学 来源:不详 题型:单选题
| A.只有①② | B.只有①③④ | C.只有①②③ | D.全部 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液各40.00mL,加热至120℃左右,使氨气全部逸出[(NH4)2SO4和NH4HSO4的分解温度均高于200℃],测得有关实验数据如下(标准状况):
SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液各40.00mL,加热至120℃左右,使氨气全部逸出[(NH4)2SO4和NH4HSO4的分解温度均高于200℃],测得有关实验数据如下(标准状况):

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.09mol的H2 | B.0.09mol的SO2 |
| C.小于0.045mol的SO2 | D.0.045mol的SO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Na2S(s)+4H2O(g) ΔH>0若反应在恒温恒容状态下进行,回答以下问题:
Na2S(s)+4H2O(g) ΔH>0若反应在恒温恒容状态下进行,回答以下问题:查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 生产过程 | 化学反应 | 反应情况 |
| 硫铁矿的燃烧 | 4 +11O2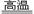 2Fe2O3+8SO2 2Fe2O3+8SO2 | 4%的硫元素损失而混入炉渣 |
| SO2的接触氧化 | 2SO2+O2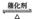 2SO3 2SO3 | SO2转化率为95% |
| SO3的吸收 | SO3+H2O=H2SO4 | SO3的吸收率为98% |
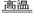 2Fe2O3+8SO2
2Fe2O3+8SO2查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SO2是硫及某些含硫化合物在空气中燃烧的产物 |
| B.SO2具有漂白性,可以使品红溶液褪色 |
| C.SO2溶于水后生成H2SO4 |
| D.SO2是一种大气污染物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.硫酸起了催化剂的作用 |
| B.硫酸起了脱水剂的作用 |
| C.硫酸吸收了氨,增大了正反应速率 |
| D.硫酸吸收了氨,减小了逆反应速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com