
同温同压下,在3支相同体积的试管中分别充有等体积混合的两种气体,它们是:①NO和NO2,②NO2和O2,③NH3和N2。现将3支试管均倒置于水槽中,充分反应后,试管中剩余气体的体积分别为V1、V2、V3,则下列关系正确的是( )
A.V1>V2>V3 B.V1>V3>V2 C.V2>V3>V1 D.V3>V1>V2
科目:高中化学 来源:2016-2017学年江西省高二12月月考化学卷(解析版) 题型:选择题
除去下列物质中的杂质(括号中为杂质),采用的试剂和除杂方法错误的是( )
序号 | 待除杂质 | 试剂 | 除杂方法 |
A | C2H4(SO2) | NaOH溶液 | 洗气 |
B | C6H6(Br2) | Fe粉 | 蒸馏 |
C | C6H5NO2(NO2) | NaOH | 分液 |
D | C2H2(H2S) | CuSO4 | 洗气 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南浏阳一中等两校高二12月联考化学卷(解析版) 题型:实验题
某常用的血液抗凝剂由(NH4)2C2O4和Na2C2O4组成,为确定其成分,某同学进行如下实验:
①氮元素测定:精确称取a g样品,加适量蒸馏水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量浓NaOH溶液,加热装置A产生水蒸气,装置B中产生的氨气全部吹出,用V1mLc1mol/L的硫酸溶液吸收。蒸氨结束后取下接收瓶,用c2mol/LNaOH标准溶液过剩的H2SO4,到终点时消耗V2mLNaOH溶液。
②C2O42-离子的测定:取实验①B装置中剩余溶液于锥形瓶中,先用稀硫酸酸化,再用0.1000mol/L的酸性KMnO4溶液滴定,终点时消耗酸性KMnO4溶液V3mL。
③计算:根据实验①计算氮元素的含量,根据②计算C2O42-的含量,从而得到样品中(NH4)2C2O4和Na2C2O4的比例。完成下列问题:
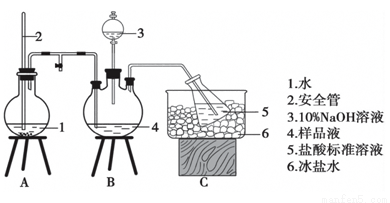
(1)装置A中长玻璃管的作用是 。
(2)用NaOH标准溶液滴定过剩H2SO4时, NaOH标准溶液盛装在 中(填仪器名称)。
(3)样品中氮元素的质量分数表达式为 。
(4)实验②中发生的离子方程式为 。用酸性高锰酸钾溶液滴定时终点现象为 。
(5)实验②中滴定开始和结束时,滴定管的读数如图所示,则所用酸性KMnO4溶液体积V3= mL
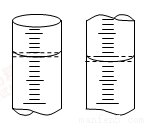
(6)下列操作可能使实验②测定结果偏低的是 。
A.滴定管在注入溶液前用蒸馏水洗后未用标准溶液润洗
B.开始时酸式滴定管尖嘴部分有气泡,滴定过程中消失
C.滴定前仰视滴定管读数,滴定后平视滴定管读数
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南浏阳一中等两校高二12月联考化学卷(解析版) 题型:选择题
下列说法中,可以说明恒容密闭容器中的反应:P(g)+Q(g) R(g)+S(g)在恒温下已达平衡状态的是 ( )
R(g)+S(g)在恒温下已达平衡状态的是 ( )
A.反应容器内压强不随时间变化
B. P和S的生成速率相等
C.反应容器内P、Q、R、S四者物质的量浓度为1:1:1:1
D.反应容器内总物质的量不随时间而变化
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高一上期末化学卷(解析版) 题型:计算题
将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。请回答:
(1)NO的物质的量为________mol,NO2的物质的量为________mol。
(2)待产生的气体全部释放后,向溶液中加入VmL、amol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为________mol·L-1。
(3)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要30%的双氧水_______g。
(书写计算过程)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高一上期末化学卷(解析版) 题型:选择题
下列各组物质在溶液中反应时,以任意比混合均能用同一离子方程式表示的是( )
A.AlCl3溶液和NaOH溶液 B.Ba(OH)2溶液与稀硫酸
C.Na2CO3溶液和稀盐酸  D.Fe和稀硝酸
D.Fe和稀硝酸
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高一上期末化学卷(解析版) 题型:选择题
已知甲、乙、丙和X是四种中学化学中常见的物质,其转化关系如下图,则甲和X不可能是( )

A.甲为C,X是O2 B.甲为SO2,X是NaOH溶液
C.甲为Cl2,X为Fe D.甲为Al,X为NaOH溶液
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上月考五化学试卷(解析版) 题型:选择题
室温下,将1 mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为ΔH1,将1 mol的CuSO4(s)溶于水会使溶液温度升高,热效应为ΔH2;CuSO4·5H2O受热分解的化学方程式为CuSO4·5H2O(s) 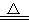 CuSO4(s)+5H2O(l),热效应为ΔH3,则下列判断正确的是( )
CuSO4(s)+5H2O(l),热效应为ΔH3,则下列判断正确的是( )
A.ΔH2>ΔH3 B.ΔH1+ΔH3=ΔH2 C.ΔH1<ΔH3 D.ΔH1+ΔH2>ΔH3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高二上期中化学卷(解析版) 题型:填空题
2016年10月17日我国神舟十一号载人飞船在酒泉卫星发射中心成功发射,为我们更好地掌握空间交会对接技术、开展地球观测活动奠定了基础。我国制造航天飞船的主要材料是铝,因而其也被称为会飞的金属,请根据其性质回答下列问题:
(1)现在工业冶炼铝的化学方程式为 。
(2)铝锂合金是今年来航空金属材料中发展最为迅速的一个领域,主要因为合金的某些性能优于各成分金属,其中包括 、 等方面。同时铝锂形成化合物LiAlH4既是金属储氢材料又是有机合成中的常用试剂,遇水能得到无色溶液并剧烈分解释放出H2,LiAlH4在化学反应中通常作
(填“氧化”或“还原”)剂。
(3)铝电池性能优越,在现代生产、生活中有广泛的应用。
①Al-Ag2O电池可用作水下动力电源,化学反应为2Al+3Ag2O+2NaOH=2NaAlO2+6Ag+H2O,则负极的电极反应式为 ,正极附近溶液的pH (填“变大”“不变”或“变小”),
②铝一空气电池以其环保、安全而受到越来越多的关注,其原理如下图所示。

该电池的负极反应方程式为 ;正极反应方程式为 ;
电池中NaCl溶液的作用是 ;以该电池为电源,用惰性电极电解Na2SO4溶液,当Al电极质量减少1.8g时,电解池阴极生成的气体在标准状况下的体积为 L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com