
| A. | 两个隔离的不同半电池通过盐桥连接可以组成原电池 | |
| B. | 电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属 | |
| C. | 在铁上镀银,用银作阳极 | |
| D. | 牺牲阳极的阴极保护法利用的是原电池原理 |
分析 A.离子通过盐桥定向移动;
B、电解精炼铜,阳极上的锌和铁也会失电子生成离子,阳极泥是银、金等;
C、电镀时镀层金属作阳极,发生氧化反应;
D、在原电池中正极被保护,负极被腐蚀.
解答 解:A.离子通过盐桥定向移动,可形成闭合回路,所以两个隔离的不同半电池通过盐桥连接可以组成原电池,故A正确;
B、电解精炼铜,阳极上的锌和铁也会失电子生成离子,阳极泥是银、金等,所以不存锌与铁,故B错误;
C、电镀时镀层金属作阳极,发生氧化反应,所以在铁上镀银,用银作阳极,故C正确;
D、在原电池中正极上溶液中的离子得电子,正极的电极材料不反应,即正极被保护,负极失电子被腐蚀,属于牺牲阳极的阴极保护法,故D正确;
故选:B.
点评 本题考查了电解池、原电池原理的分析判断,电极反应和电极判断是解题关键,掌握基础是关键,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 海水分解 | |
| B. | 温度升高,其他溶质的溶解度增大 | |
| C. | 升高温度,降低食盐在水中的溶解度 | |
| D. | 利用阳光、风力蒸发水分使氯化钠成晶体析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
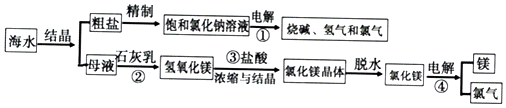
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
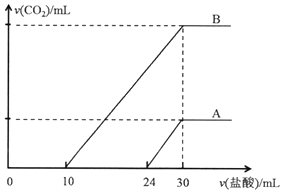 向两份30ml同一浓度的NaOH溶液中通入CO2气体,因CO2通入量的不同,溶液的组成也不同,得到溶液M、N.若向M、N溶液中逐滴加入浓度为0.25mol•L-1盐酸,产生的气体体积v(CO2)与加入盐酸的体积v(HCl)的关系分别为如图所示两种情况A和B.
向两份30ml同一浓度的NaOH溶液中通入CO2气体,因CO2通入量的不同,溶液的组成也不同,得到溶液M、N.若向M、N溶液中逐滴加入浓度为0.25mol•L-1盐酸,产生的气体体积v(CO2)与加入盐酸的体积v(HCl)的关系分别为如图所示两种情况A和B.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 物质 | 用途 |
| A | 硅单质 | 制作光导纤维 |
| B | 烧碱 | 治疗胃酸过多 |
| C | 铁罐车 | 常温下用于运输浓硝酸 |
| D | 液氨 | 用作消毒剂 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上第一次教学诊断化学卷(解析版) 题型:选择题
已知:还原性HSO3->I-,氧化性IO3->I2。在含3 mol NaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和析出的I2的物质的量的关系曲线如图(不考虑I2+I-  I3-)下列说法不正确的是
I3-)下列说法不正确的是
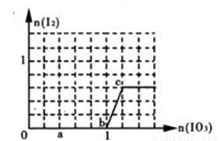
A.a点时消耗NaHSO3的物质的量为1.2mol,得到的氧化产物为SO42-
B.b~c段的反应可用如下离子方程式表示:IO3-+5I-+6H+=3I2+3H2O
C.滴加过程中水的电离平衡一直逆向移动。
D.从c点后所得混合液中分离出碘的操作为:加四氯化碳萃取分液,然后蒸馏
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com