
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.水电离出的c(H+)·c(OH-)=10-22的溶液:K+、Na+、SO 、S2O
、S2O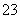
B.澄清透明溶液:Mg2+、Cu2+、Cl-、SO
C.使酚酞变红色的溶液:NH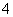 、K+、AlO
、K+、AlO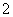 、NO
、NO
D.含0.1 mol·L-1KI的溶液:Fe2+、Na+、NO 、Cl-
、Cl-
科目:高中化学 来源: 题型:
某有机物的结构简式为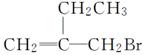 。下列关于该物质的说法中正确的是( )
。下列关于该物质的说法中正确的是( )
A.该物质可以发生水解反应
B.该物质能和AgNO3溶液反应产生AgBr沉淀
C.该物质可以发生消去反应
D.该物质分子中至多有4个碳原子共面
查看答案和解析>>
科目:高中化学 来源: 题型:
能在水溶液中大量共存的离子组是( )
A.H+、Fe3+、SO 、I-
、I-
B.H+、NH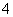 、HCO
、HCO 、NO
、NO
C.Ag+、K+、Cl-、SO
D.K+、AlO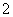 、Cl-、OH-
、Cl-、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
水溶液中能大量共存的一组离子是( )
A.Na+、Ca2+、Cl-、SO
B.Fe2+、H+、SO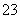 、ClO-
、ClO-
C.Mg2+、NH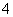 、Cl-、SO
、Cl-、SO
D.K+、Fe3+、NO 、SCN-
、SCN-
查看答案和解析>>
科目:高中化学 来源: 题型:
水溶液中能大量共存的一组离子是( )
A.Na+、AlO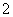 、Cl-、HCO
、Cl-、HCO
B.H+、S2-、Cl-、SO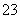
C.H+、Mg2+、Cl-、NO
D.K+、Ag+、OH-、SO
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物A、B是中学常见的物质,其阴、阳离子只能从下表中选择:
| 阳离子 | K+、Na+、Fe2+、Ba2+、NH |
| 阴离子 | OH-、NO |
(1)若A、B的水溶液均为无色,且A的水溶液呈强酸性,B的水溶液呈强碱性。混合后产生不溶于稀盐酸的白色沉淀及能使湿润的红色石蕊试纸变蓝色的气体。
①B的化学式为______________。
②A、B溶液混合加热反应的离子方程式为________________________________________________________________________。
(2)若A的水溶液呈浅绿色,B的水溶液无色且其焰色反应为黄色。向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合亦无明显变化。则
①A的化学式为______________。
②经分析上述过程中溶液变黄的原因可能有两种(用离子方程式表示)
Ⅰ________________________________________________________________________;
Ⅱ________________________________________________________________________。
③请用一简易方法证明上述溶液变黄的原因________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
铝是中学化学学习阶段的唯一一种既能与酸(非氧化性酸)反应又能与强碱溶液反应放出H2的金属,就铝的这一特殊性质回答下列问题:
(1)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得H2的体积之比是________。
(2)足量的两份铝分别投入到等体积、等物质的量浓度的盐酸、氢氧化钠溶液中,产生H2的体积之比是________。
(3)足量的两份铝分别投入到等体积、一定物质的量浓度的HCl、NaOH溶液中,二者产生的H2相等,则HCl和NaOH的物质的量浓度之比是________。
(4)甲、乙两烧杯中各盛有100 mL 3 mol·L-1的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后,测得生成的气体体积比为V(甲)∶V(乙)=1∶2,则加入铝粉的质量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
铝土矿的主要成分为氧化铝、氧化铁和二氧化硅,工业上经过下列工艺可以冶炼金属铝:


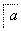

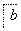 ,③
,③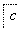 ,④
,④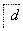 电解,
电解,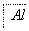
下列说法中错误的是( )
A.①②中除加试剂外,还需要进行过滤操作
B.a、b中铝元素的化合价相同
C.③中需要通入过量的氨气
D.④进行的操作是加热,而且d一定是氧化铝
查看答案和解析>>
科目:高中化学 来源: 题型:
已知五种元素的原子序数的大小顺序为C>A>B>D>E;A、C同周期;B、C同主族;A与B形成离子化合物,A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子分子,试回答下列问题:
(1)写出五种元素的名称:
A__________,B__________,C__________,
D__________,E__________。
(2)写出A、B形成的AB型离子化合物与CO2反应的化学方程式。
(3)写出D元素形成的单质的结构式
(4)C、E元素形成化合物的空间构型为。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com