
A.Al3+、SO2-4 、NH3·H2O、Cl- 、NH3·H2O、Cl- | B.Na+、NO-3、H+、Fe2+ | C.K+、Fe3+、H2SO3、SCN- | D.K+、OH-、NO-3、AlO2或[Al(OH)4] |
 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源:不详 题型:单选题
| A.室温下,由水电离出c(OH-)=1×10-12 mol·L-1的溶液中:K+、HCO3-、Na+、Cl- |
| B.含有0.1 mol·L-1 Fe2+的溶液中:NH4+、SO42-、H+、NO3- |
| C.澄清透明的溶液中:Cu2+、Mg2+、SO42-、Cl- |
| D.室温下,pH=1的溶液中:Na+、Cl-、K+、CH3COO- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.钠与水反应 2Na+2H2O = 2Na+ + 2OH- + H2↑ |
| B.氢氧化镁与硫酸溶液反应 OH-+H+=H2O |
| C.碳酸钙与醋酸溶液反应: CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑ |
| D.铁与稀硫酸反应 2Fe+6H+=2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
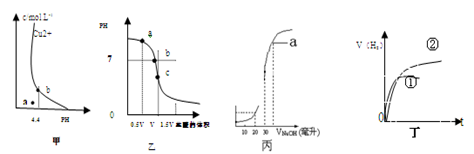
A.图甲表示某温度下,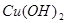 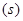 在溶液中达到沉淀溶解平衡后,改变溶液PH, 在溶液中达到沉淀溶解平衡后,改变溶液PH,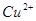 浓度的变化。由图可知 浓度的变化。由图可知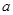 点溶液未达到饱和,因此, 点溶液未达到饱和,因此,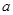 点的 点的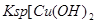 ]小于 ]小于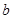 点。 点。 |
B.图乙表示在室温时用一定浓度的盐酸滴定V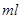 同浓度的氨水。 同浓度的氨水。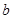 点时溶液中 点时溶液中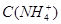 = =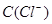 ,且溶液中水的电离程度最大。 ,且溶液中水的电离程度最大。 |
C.图丙表示在室温时,用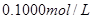 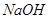 溶液滴定30.00ml0.1mol/L 溶液滴定30.00ml0.1mol/L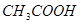 溶液,点a所示溶液中C( 溶液,点a所示溶液中C(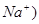 > >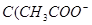 )> )>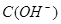 > >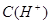 |
D.图丁可表示同体积同PH的某一元强酸溶液①和某一元中强酸溶液②分别与足量的锌粉发生反应生成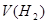 随时间( 随时间( )的变化情况。 )的变化情况。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
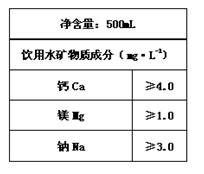
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碳酸钙溶于过量的乙酸:CaCO3+2H+=Ca2++CO2↑+H2O |
| B.氟气与水反应:F2+H2O===H++F-+HFO |
| C.溴化亚铁溶液中通人少量氯气:2Fe2++C12=2Fe3++2Cl- |
D.向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体:Fe3++3H2O 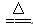 Fe(OH)3↓+3H+ Fe(OH)3↓+3H+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NH4+、NO3-、Al3+、I- | B.Na+、Al3+、K+、NO3- |
| C.Cu2+、K+、SO42-、Na+ | D.K+、SO42-、HCO3-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com