
对已达化学平衡的下列反应 2X(g)+Y(g)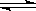 2Z(g)减小压强时,对反应产生的影响是( )
2Z(g)减小压强时,对反应产生的影响是( )
A 逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B 逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C 正、逆反应速率都减小,平衡向逆反应方向移动
D 正、逆反应速率都增大,平衡向正反应方向移动
科目:高中化学 来源: 题型:
某中性有机物C8H16O2在稀硫酸作用下加热得到M和N两种物质,N经氧化最终可得到M,则该中性有机物的结构可能有( )
A.1种 B.2种
C.3种 D.4种
查看答案和解析>>
科目:高中化学 来源: 题型:
实验是化学研究的基础,下列关于各实验装置的叙述正确的是( )
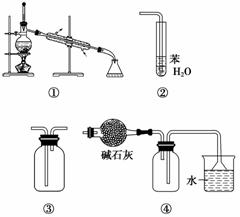
A.装置①常用于分离互相溶解且沸点相差不大的液态混合物
B.装置②可用于吸收NH3或HCl气体,并防止倒吸
C.装置③可用于收集H2、CO2、Cl2、NH3等气体
D.装置④可用于干燥、收集氨气,若将碱石灰改成五氧化二磷,可用于干燥、收集氯化氢
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃、1.01×105Pa,反应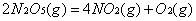 △H = + 56.76kg/mol能自发进行的原因是
△H = + 56.76kg/mol能自发进行的原因是
A 是吸热反应 B 是放热反应
C是熵减少的反应 D 熵增大效应大于能量效应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列热化学方程式中,△H能正确表示物质的燃烧热的是
A. CO(g) +1/2O2(g) ==CO2(g) △H=-283.0 kJ/mol
B. C(s) +1/2O2(g) ==CO(g) △H=-110.5 kJ/mol
C. H2(g) +1/2O2(g)==H2O(g) △H=-241.8 kJ/mol
D. 2C8H18(l) +25O2(g)==16CO2(g)+18H2O(l) △H=-11036 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
| 物质 | X | Y | Z |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是
A.增大压强使平衡向生成Z的方向移动,平衡常数增大
 B.反应可表示为X+3Y 2Z,其平衡常数为1600
B.反应可表示为X+3Y 2Z,其平衡常数为1600
C.反应达到平衡时,X的转化率为50%
D.改变温度可以改变此反应的平衡常数
查看答案和解析>>
科目:高中化学 来源: 题型:
已知 C(s)+1/2O2(g)==CO(g) ΔH1=-110.5kJ/mol
2CO(g)+O2(g)== 2CO2(g) ΔH2=-566.0kJ/mol
试写出固态碳和氧气反应生成二氧化碳的热化学反应方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上制硫酸时的一步主要反应是在接触室中生成SO3的反应:
2SO2(g)+O2(g)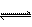 2SO3(g); △H<0,该反应的条件选择如下,其中可以完全用勒夏特列原理解释的是
2SO3(g); △H<0,该反应的条件选择如下,其中可以完全用勒夏特列原理解释的是
A.使用催化剂 B.400℃~500℃的高温 C.O2过量 D.采用常压
查看答案和解析>>
科目:高中化学 来源: 题型:
已知H2(g)+Cl2(g)=2HCl(g),ΔH = —184.6 kJ·mol-1
则反应HCl(g)= 1/2H2(g)+1/2Cl2(g)的ΔH是
A.+184.6kJ·mol-1 B.—369.2 kJ·mol-1
C.+92.3 kJ·mol-1 D.—92.3 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com