
| A. | 甲醛是甲基跟醛基相连而构成的 | |
| B. | 饱和一元醛的通式可简写为RCOH | |
| C. | 在银镜反应中乙醛体现了氧化性 | |
| D. | 饱和一元脂肪醛的分子组成符合通式CnH2nO |
分析 A.甲醛是H与醛基相连而成的;
B.饱和一元醛的通式可简写为RCHO;
C.乙醛含有醛基,在发生银镜反应时表现了还原性;
D.根据饱和一元醛是指含有一个醛基,烃基为不存在不饱和键进行分析.
解答 解:A.甲醛是H与醛基相连而成的,乙醛是甲基跟醛基相连而构成的,故A错误;
B.饱和一元醛的通式可简写为RCHO,醛基不能写为-COH,故B错误;
C.乙醛含有醛基,在发生银镜反应时表现了还原性,故C错误;
D.饱和一元醛是指含有一个醛基,烃基为不存在不饱和键,饱和一元醛通式为:CnH2nO,故D正确;
故选D.
点评 本题考查醛类物质的结构和性质,题目难度不大,注意醛基的正确写法和掌握饱和一元醛通式的确定方法.


 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 新制氯水的酸性强 | B. | 新制氯水的酸性弱 | ||
| C. | 久置氯水中无氯分子 | D. | 久置氯水已无漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使高分子材料具有仿生能力 | |
| B. | 使高分子材料向功能材料方向发展 | |
| C. | 使高分子材料越来越牢固,难分解 | |
| D. | 使农用薄膜能够选择性地透过某种植物所需要的特定波长的光 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
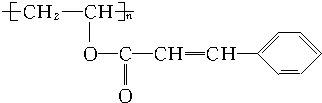
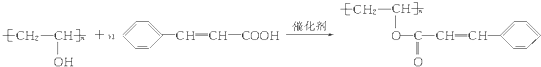 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
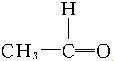 +
+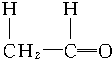 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$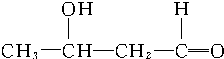
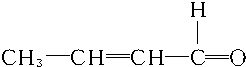 +2H2$→_{△}^{催化剂}$
+2H2$→_{△}^{催化剂}$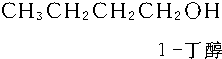
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
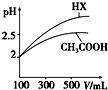 已知25℃时部分弱电解质的电离平衡常数数据如表所示:
已知25℃时部分弱电解质的电离平衡常数数据如表所示:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V1:V2的值 | B. | V1和V2的值 | ||
| C. | X和Y的物质的量 | D. | 盐酸和稀硫酸的物质的量浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
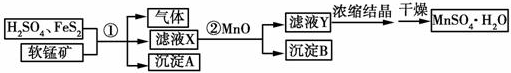
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com