

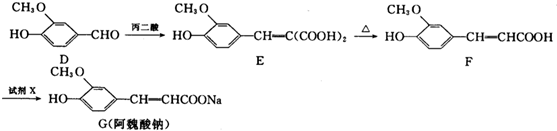
| 丙二酸 |
| 水 |
| △ |
| 水 |
| △ |
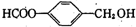 等,故答案为:
等,故答案为: 等.
等.


科目:高中化学 来源: 题型:
| A、溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+=AgBr↓ | ||
| B、用醋酸除去水垢:CaCO3+2H+=Ca2++H2O+CO2↑ | ||
| C、苯酚与纯碱溶液混合:2C6H5OH+CO32-→CO2↑+H2O+2C6H5O- | ||
D、甲醛溶液与足量的银氨溶液共热HCHO+4Ag(NH3)2++4OH-
|
查看答案和解析>>
科目:高中化学 来源: 题型:
 某研究性学习小组为探究Cl2的氧化性和I-的还原性强于Fe2+,设计了如图装置制取Cl2,并进行实验探究.回答下列问题:
某研究性学习小组为探究Cl2的氧化性和I-的还原性强于Fe2+,设计了如图装置制取Cl2,并进行实验探究.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在AgBr饱和溶液中加入AgNO3溶液,达到平衡时,溶液中Br-浓度降低 |
| B、常温下,pH=4的溶液一定是酸溶液 |
| C、FeCl3溶液和Fe2(SO4)3溶液加热蒸干、灼烧都得到Fe2O3 |
| D、在滴有酚酞的Na2CO3溶液中加入BaCl2溶液,溶液褪色,说明BaCl2溶液有酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向Ag2CrO4的浊液中加入AgNO3溶液,Ag2CrO4的Ksp减小 |
| B、将0.001 mol?L-1的AgNO3溶液逐滴加入到含Cl-和CrO42-浓度均为0.001 mol?L-1的溶液中,则先产生AgCl沉淀 |
| C、饱和AgCl溶液与饱和Ag2CrO4溶液相比,前者的c(Ag+)大 |
| D、该温度下,AgCl在水中的溶解度小于在食盐水中的溶解度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com