
下列微粒结构示意图中,不正确的是

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2013-2014江西省高一下学期期末考试化学试卷(解析版) 题型:选择题
某元素只存在两种天然同位素,且在自然界它们的含量相近,其相对原子质量为152.0,原子核外的电子数为63。下列叙述中错误的是( )
A.它是副族元素 B.它是第六周期元素
C.它的原子核内有63个质子 D.它的一种同位素的核内有89个中子
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省上饶市第二学期期末教学质量测试高二化学试卷(解析版) 题型:选择题
如图所示装置中,a?b都是惰性电极,通电一段时间后(电解液足量),a极附近溶液显红色?下列说法正确的是

A.a是负极,b是正极
B.CuSO4溶液的pH逐渐减小
C.铜电极上的反应式为
D.向NaCl溶液中加入一定量的盐酸,能使溶液与原来溶液完全一样
查看答案和解析>>
科目:高中化学 来源:2013-2014江西八一中学、洪都中学下学期期中考试高一化学试卷(解析版) 题型:选择题
下列说法正确的是
A.离子键就是使阴、阳离子结合成化合物的静电引力
B.所有金属与所有非金属之间都能形成离子键
C.在化合物CaCl2中,两个氯离子之间也存在离子键
D.含有离子键的化合物一定是离子化合物
查看答案和解析>>
科目:高中化学 来源:2013-2014江西八一中学、洪都中学下学期期中考试高一化学试卷(解析版) 题型:选择题
有关氨的说法不正确的是
A.NH3是4核10电子的分子,三角锥形,具有还原性
B.NH3极易溶于水,可做喷泉实验;氨气易液化,液氨可用作制冷剂
C.氨气是非电解质,氨水是电解质
D.蘸有浓盐酸的玻璃棒遇氨气可产生白烟
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省盐城市高二下学期期终考试化学试卷(解析版) 题型:实验题
(12分)某学生用0.1000mol·L-1标准NaOH溶液滴定未知浓度的盐酸,其操作可分解为以下几步:
A移取25.00mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞溶液
B用标准NaOH溶液润洗滴定管2~3次
C把盛有标准NaOH溶液的碱式滴定管固定好,挤压玻璃珠,使滴定管尖嘴充满溶液
D取标准NaOH溶液注入碱式滴定管到“0”刻度以上2~3cm
E.调节液面至“0”或“0”刻度以下,记下读数
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定到终点,并记下滴定管液面的读数
(1)下图中属于碱式滴定管的 (选填:“甲”、“乙”)。

(2)正确的操作顺序是 (填字母序号)。
(3)上述B步操作的目的是 。
(4)判断到达滴定终点的实验现象是 。
(5)上述A步操作之前,若先用待测溶液润洗锥形瓶,则对滴定结果的影响是 (填“偏大”或“偏小”或“无影响”)。
(6)若平行实验三次,记录的数据如下表
滴定次数 | 待测溶液的体积(/mL) | 标准NaOH溶液的体积 | |
滴定前读数(/mL) | 滴定后读数(/mL) | ||
1 | 25.00 | 1.02 | 21.03 |
2 | 25.00 | 2.00 | 21.99 |
3 | 25.00 | 0.20 | 20.20 |
试计算待测盐酸的物质的量浓度(列出计算过程)。
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省盐城市高二下学期期终考试化学试卷(解析版) 题型:选择题
对羟基苯甲醛(结构简式如图)是医药工业和香料工业的重要中间体。下列说法不正确的是

A.能发生水解反应
B.有两种含氧官能团
C.与苯甲酸(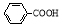 )互为同分异构体
)互为同分异构体
D.一定条件下能与溴水、FeCl3溶液及银氨溶液反应
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省盐城市高一下学期期末考试化学试卷(解析版) 题型:选择题
绿色化学要求利用化学反应原理从源头上消除污染。以铜为原料制备硫酸铜,下列四种原理设计,其中最能体现“绿色化学”要求的是
A.Cu +2H2SO4(浓)  CuSO4 +SO2↑+2H2O
CuSO4 +SO2↑+2H2O
B.Cu +Cl2  CuCl2 ,CuCl2+ H2SO4(浓)
CuCl2 ,CuCl2+ H2SO4(浓)  CuSO4 +2HCl↑
CuSO4 +2HCl↑
C.Cu + H2SO4 +H2O2  CuSO4 +2H2O
CuSO4 +2H2O
D. 3Cu +8HNO3=3Cu(NO3)2 +2NO↑+4H2O,Cu(NO3)2+H2SO4(浓)  CuSO4 +2HNO3↑
CuSO4 +2HNO3↑
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省第二学期期中考试高一化学试卷(解析版) 题型:填空题
(24分)下表是元素周期表的一部分,针对表中①~⑩种元素,填写下列空白:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 |
|
|
| ① | ② | ③ | ④ |
|
3 | ⑤ | ⑥ | ⑦ |
|
|
| ⑧ |
|
4 | ⑨ | ⑩ |
|
|
|
|
|
|
(1)被选作相对原子质量标准的核素是 (填核素符号)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是 ,碱性最强的化合物的化学式是 。
(3)最高价氧化物是两性氧化物的元素在第 族;写出它的氧化物与氢氧化钠溶液反应的离子方程式 。
(4)从⑤到⑧的元素中, 原子半径最大(填元素符号)。
(5)元素④与⑥形成的化合物属于 (填 “共价”或“离子”)化合物。
(6)若要比较⑤比⑥的金属性强弱,下列实验方法可行的是 。
A、将单质⑤置于⑥的盐溶液中,如果⑤不能置换出单质⑥,说明⑤的金属性弱
B、比较⑤和⑥的最高价氧化物对应水化物的水溶性,前者比后者溶解度大,故前者金属性强
C、将⑤、⑥的单质分别投入到水中,观察到⑤与水反应更剧烈,说明⑤的金属性强
D、将⑤、⑥的单质分别在O2中燃烧,前者得到氧化物的颜色比后者得到氧化物的颜色深,则前者金属性强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com