
����Ŀ���穁Fenton��������ˮ�����л���Ⱦ�オ��ĸ������������䷴Ӧԭ����ͼ��ʾ�����е�������H2O2��Fe2+����Fenton��Ӧ��Fe2++H2O2=Fe3++OH��+OH�����ɵ��������ɻ���OH�������������л���Ⱦ�����˵������ȷ���ǣ� �� 
A.��Դ��A���Ǹ���
B.������ֻ��O2��Fe3+������ԭ��Ӧ
C.�����Ϸ����缫��Ӧ��H2O��e��=OH+H+ ��
D.����1molO2 �� ���Բ���4molOH
���𰸡�B
���������⣺A����Դ��A�缫���ӵĵ缫�Ϸ����õ��ӵĻ�ԭ��Ӧ����õ缫Ϊ����������AΪ��������A��ȷ�� B��O2��Fe3+�������ϵõ��ӷ�����ԭ��Ӧ��H2O2���������ӷ�Ӧ����H2O2�����õ��ӵĻ�ԭ��Ӧ����B����
C��������ˮʧ���������ǻ��������ӣ���缫����ʽΪ��H2O��e��=OH+H+ �� ��C��ȷ��
D��1molO2ת��Ϊ2molH2O2ת��2mole�� �� ��Fe2++H2O2=Fe3++OH��+OH��֪������2molOH��ת��2mole�� �� ������������2molOH����������1molO2 �� ���Բ���4molOH����D��ȷ��
��ѡB��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D���ֶ�����Ԫ�أ�0.5molA��Ԫ�ص����ӵõ�NA�����Ӻ�ԭΪ����ԭ�ӣ�0.4gA��������ǡ����100mL0.2mol/L��������ȫ��Ӧ��AԪ��ԭ�Ӻ�������������������ȣ�BԪ��ԭ�Ӻ����������AԪ��ԭ�Ӻ����������1��C�����Ӻ�����Ӳ�����AԪ�ص����Ӻ�����Ӳ�����1��DԪ��ԭ�������������Ǵ�����������2������1��AԪ�صķ�������2��B�ĵ�����C��D ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�顱�ǽ�һ֧��С���Թ�װ����һ�Թ��У�����װ�����ԭ����Ҫ��֧������Թܽ��е�ʵ�顣�����������ŵ㣬���������㷺������Ӧ���ڻ�ѧʵ���С��������ʵ��Ϊ����ʵ�顱��ʵ��װ����ͼ��С�Թ��в���մ����ˮ����ͭ��ĩ����֬�ޡ���۲�ʵ��װ�ã�����ʵ��ԭ�������ش��������⣺
��1������ʵ������У��ܹ۲쵽������Ϊ��
���ձ�A������С�Թ�����
���ձ�B����
��2��ʵ�����ʱ���ڲ�����Ҫ�ر�ע��������ǣ�
��3��д��ʵ������з�����Ӧ�Ļ�ѧ����ʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ�Ǿ����Դ���⣬�Ӻ�ˮ����ȡʳ�κ���Ĺ�����ͼ1�� 
��1�����оٺ�ˮ���������ַ������� ��
��2������I�м����Br2 �� ����II���ֽ�Br2��ԭΪBr�� �� ��Ŀ���� ��
��3������II��SO2ˮ��Һ����Br2 �� �����ʿɴ�95%���йط�Ӧ�����ӷ���ʽΪ ��
��4��ij��ѧ�о���ѧϰС��Ϊ���˽�ӹ�ҵ�����ᴿ��ķ������������й�����֪��Br2�ķе�Ϊ59�森����ˮ���ж�����ǿ��ʴ�ԣ����Dzι��������̺�����ͼ2װ�ü�ͼ�� 
�������������ۣ�
��ͼ������B�������� ��
������ʵ��װ�����������Ӿ��������������ܣ���ԭ���� ��
��ʵ��װ�����������ã�Ҫ�ﵽ�ᴿ���Ŀ�ģ���������ο��ƹؼ������� ��
��C��Һ����ɫΪ �� Ϊ��ȥ�ò������Բ���������Cl2 �� �������м���NaBr����Һ����ַ�Ӧ���ٽ��еķ�������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���ŨH2SO4��˵����ȷ����
A.��һ����ɫճ��״��Һ��B.������ʹCu�����ۻ�
C.ʹ���DZ����������ˮ��D.�����ڸ��ﰱ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��I������ʧ��֢ҩ�������氷���м��壬��ϳ�·�����£� 
��1����Ӧ�ٵ�����Ϊ�� �� ��Ӧ�ܵ�����Ϊ�� ��
��2������F�к��������ŵ�����Ϊ ��
��3����Ӧ�ۻ�������D��Ϊͬ���칹��ĸ�����÷�Ӧ�ķ���ʽΪ ��
��4����δ��Ʒ�Ӧ�ޣ�����I�п��ܻ������ʣ�������ͬ������һ����Ԫ����������Ԫ������ṹ��ʽΪ ��
��5��д��ͬʱ������������������I��һ��ͬ���칹��Ľṹ��ʽ �� ���ܷ���������Ӧ�����ܷ���ˮ�ⷴӦ���۷��ӵĺ˴Ź���������5���壮
��6����֪��CH2=CHCH2OH ![]() CH2=CHCOOH ��CH2=CHCH=CH2��
CH2=CHCOOH ��CH2=CHCH=CH2��  Ϊԭ�ϣ��ϳ�
Ϊԭ�ϣ��ϳ�  ��д���ϳ�����ͼ�����Լ����ã����ϳ�
��д���ϳ�����ͼ�����Լ����ã����ϳ�
����ͼʾ�����£�CH2=CH2 ![]() CH3CH2Br
CH3CH2Br ![]() CH3CH2OH�� ��
CH3CH2OH�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��800��ʱ����2L���ܱ������з�����Ӧ��2NO��g��+O2��g��2NO2 �� n��NO����ʱ��ı仯�����ʾ��
ʱ��Ms | 0 | 1 | 2 | 3 | 4 | 5 |
n��NO���Mmol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
��1����0��3s�ڣ���NO��ʾ��ƽ����Ӧ����v��NO��= ��
��2��ͼ�б�ʾNOŨ�ȱ仯��������������ĸ���ţ��� 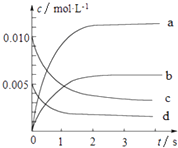
��3����ƽ��ʱNO��ת����Ϊ ��
��4����˵���÷�Ӧ�Ѵﵽƽ��״̬����������ţ��� A������������ɫ���ֲ���
B�����������ܶȱ��ֲ���
C��v�� ��NO2��=2v�� ��O2��
D����������ƽ����Է����������ֲ���
��5�������µ�850�棬��ƽ���n��NO��=n��NO2������Ӧ���������Ӧ�����淴Ӧ�����ƶ���
��6������һ��������0.2molNO������������Ӧ����ƽ��ʱ��÷ų�������ΪakJ����ʱNOת����Ϊ80%����2molNO������ȫ��Ӧ�ų�������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�ط��š���Ӧ����ʽ���ṹʾ��ͼ������ʽ���ṹʽ��ͨ��������ѧ��������йػ�ѧ����ı�ʾ��������ȷ���ǣ� ��
A.��ԭ�ӵ�ԭ�ӽṹʾ��ͼ�� ![]()
B.NH4Cl�ĵ���ʽ�� ![]()
C.ԭ�Ӻ�����10�����ӵ���ԭ�ӣ� ![]() O
O
D.�õ���ʽ��ʾ�Ȼ�����ӵ��γɹ��̣� ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������20mL0.1mol/LHA��Һ����μ���0.1mol/LNaOH��Һ����pH�仯�����ͼ��ʾ�������¶ȱ仯��������˵���в���ȷ���ǣ� �� 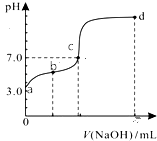
A.�����֪HAΪ����
B.�ζ��յ�λ��c��d��֮��
C.�ζ���b��ʱ��n��Na+��+n��H+����n��OH����+n��HA��=0.002mol
D.�ζ���d��ʱ��c��OH������c��Na+����c��A������c��H+��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com