
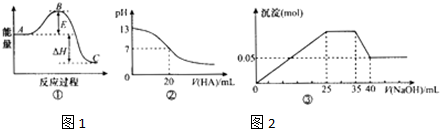
| A、若图①中曲线表示3H2(g)+N2(g)?2NH3(g),反应过程的能量变化.则升温或使用催化剂,均会使B点降低,反应速率加快 | B、图②可表示25℃时,用0.1mol/L的CH3COOH溶液滴定20mL 0.1mol/L NaOH溶液,溶液的pH随加入的酸的体积的变化情况 | C、若图③表示向含Mg2+、Al3+、NH4+、Cl-的溶液中滴加NaOH溶液时,沉淀量随NaOH溶液加入量的变化情况,则使用的NaOH溶液的浓度为10mol/L | D、若图③表示向含Mg2+、Al3+、NH4+、Cl-的溶液中滴加NaOH溶液时,沉淀量随NaOH溶液加入量的变化情况,则n(Mg2+):n(Al3+ ):n(NH4+)=2:3:2 |
| 0.1mol |
| 0.01L |


科目:高中化学 来源:2012年沪科版高中化学3.2离子键练习卷(解析版) 题型:选择题
关于化学键的下列表述中,正确的是 ( )
A.离子化合物一定含共价键 B.共价化合物可能含离子键
C.离子化合物中只含离子键 D.共价化合物中不含离子键
查看答案和解析>>
科目:高中化学 来源:2012年鲁科版高中化学选修3 2.3离子键、配位键与金属键练习卷(解析版) 题型:选择题
关于化学键的下列表述中,正确的是 ( )
A.离子化合物一定含共价键 B.共价化合物可能含离子键
C.离子化合物中只含离子键 D.共价化合物中不含离子键
查看答案和解析>>
科目:高中化学 来源:2013届山西省高二下学期期中考试理科化学试卷(解析版) 题型:选择题
在一定温度下,容器内某一反应中M、N的物质的量随反应时间的变化曲线如图,下列表述中不正确的是

A.反应的化学方程式为:2M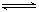 N
N
B.t3时,正逆反应速率相等
C.t2时,N的消耗速率大于N的生成速率
D.t1时,N的浓度是M浓度的2倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com