

分析 甲装置制备二氧化硫,己装置制备氯气,二氧化硫与氯气在丙中反应生成SO2Cl2,丙中活性炭可能起催化剂作用,SO2Cl2遇水发生剧烈的水解反应,乙为干燥二氧化硫,戊是饱和食盐水,降低氯气溶解度,丁干燥氯气,SO2Cl2沸点低、易挥发,B为冷凝管,使挥发的产物SO2Cl2冷凝回流,碱石灰吸收为反应的二氧化硫、氯气,防止污染空气,并吸收空气中的水蒸气,防止进入C中导致磺酰氯水解,
(1)根据装置内外压强差形成气泡或水柱分析;
(2)SO2Cl2沸点低、易挥发,B为冷凝管,使挥发的产物SO2Cl2冷凝回流,说明SO2与氯气之间的反应属于放热反应;仪器C吸收尾气;
(3)甲装置制备二氧化硫,Cu与浓硫酸反应需要加热,稀硝酸与硫酸钠不反应;
(4)分离沸点不同的液体可以用蒸馏的方法;
(5)①SO2Cl2与NaOH溶液反应生成硫酸钠和氯化钠;
②氯离子与银离子反应生成不溶液硝酸的氯化银沉淀,注意应先加入硝酸钡溶液,先排除硫酸根离子的干扰;
(6)Li失电子为负极,SOCl2为正极,正极上发生得电子的还原反应,据此书写.
解答 解:(1)检验己装置气密性的方法是:关闭分液漏斗活塞,将导管末端插入水中,加热烧瓶,导管口有气泡产生,停止加热,导管内形成一段高于液面的稳定水注,则气密性好;
故答案为:关闭分液漏斗活塞,将导管末端插入水中,加热烧瓶,导管口有气泡产生,停止加热,导管内形成一段高于液面的稳定水注,则气密性好;
(2),因冷凝管的作用是冷凝回流而反应又没有加热,故SO2与氯气间的反应为放热反应,由于会有一部分Cl2、SO2通过冷凝管逸出,故C中应使用碱性试剂,又因SO2Cl2遇水易水解,故碱石灰是用于吸收氯气、SO2并防止空气中的水蒸气进入B中;
故答案为:<;吸收尾气Cl2、SO2,防止环境污染,同时防止空气中的水蒸气进入引起磺酰氯水解;
(3)甲装置制备二氧化硫,Cu与浓硫酸反应需要加热,稀硝酸与硫酸钠不反应,60%硫酸与亚硫酸钾不需要加热可以得到二氧化硫;
故答案为:c;
(4)分离沸点不同的液体可以用蒸馏的方法,所以丙中混合物分离开的实验操作是蒸馏;
故答案为:蒸馏;
(5)①SO2Cl2与NaOH溶液反应生成硫酸钠和氯化钠,离子方程式为:SO2Cl2+4OH-=2Cl-+SO42-+2H2O;
故答案为:SO2Cl2+4OH-=2Cl-+SO42-+2H2O;
②要检验溶液中的氯离子应排除硫酸根离子的干扰,所以:取少量该溶液于试管中,加入过量Ba(NO3)2溶液,静置,向上层清液加入硝酸酸化的AgNO3溶液,若产生白色沉淀,则说明溶液中有Cl-;
故答案为:取少量w于试管中,加入足量Ba(NO3)2溶液,静置,向上层清液加入硝酸酸化的AgNO3溶液,有白色沉淀生成,则w中存在Cl-;
(6)Li失电子为负极,SOCl2为正极,正极上发生得电子的还原反应,则正极电极方程式为:SO2Cl2+2e-=SO2↑+2Cl-;
故答案为:SO2Cl2+2e-=SO2↑+2Cl-.
点评 本题考查实验制备方案,为高考常见题型,侧重于学生的分析、实验和计算能力的考查,题目涉及对反应原理、装置及操作的分析评价、离子检验、物质的分离提纯、原电池原理等,注意对物质性质信息的应用,难度中等


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.225mol/L | B. | 0.25mol/L | C. | 0.45mol/L | D. | 0.55mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
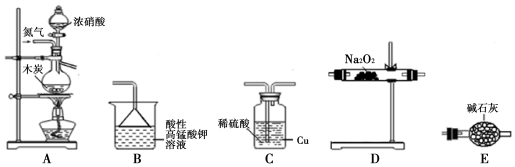
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
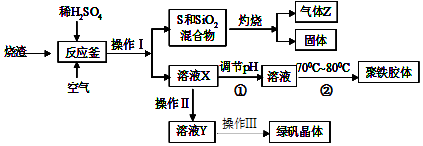
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同一周期元素形成的简单离子的半径从左到右依次减小 | |
| B. | 主族元素的最高正价均等于其族序数 | |
| C. | 元素的非金属性、金属性与元素原子在氧化还原反应中得失电子数目的多少无关 | |
| D. | 元素的非金属性越强,其气态氢化物的还原性越弱,其气态氢化物的酸性也越弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稳定性:HCl>H2S>H2O | B. | 碱性:NaOH>KOH>Mg(OH)2 | ||
| C. | 酸性:HClO4>HBrO4>HIO4 | D. | 还原性:I-<Br-<Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验目的或结论 | |
| A | 蘸有浓硝酸的玻璃棒靠近浓氨水时冒白烟 | NH3具有还原性 |
| B | 将一块Na放入乙醇溶液中,有气泡产生 | Na能置换乙醇中的氢 |
| C | 可将58.5gNaCl加入盛有500mL水的烧杯中,搅拌、溶解 | 粗略配置浓度为2mol•L-1的NaCl溶液 |
| D | 向氯仿中加入NaOH溶液,加热充分反应后,再加入AgNO3 | 验证氯仿中含有的氯元素 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com