
 ②甲苯 ③ClCH=CHCl ④
②甲苯 ③ClCH=CHCl ④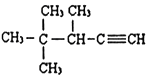
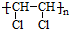
 .
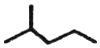
. 分析 (1)①为2-甲基戊烷;③含有碳碳双键,可发生加聚反应;
(2)④含有碳碳三键、主链为5个C原子;
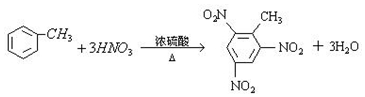
(3)甲苯苯环有5个H原子可被取代,TNT为三硝基甲苯.
解答 解:(1)①为2-甲基戊烷,分子式为C6H14;③含有碳碳双键,可发生加聚反应,加聚产物为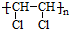 ,故答案为:C6H14;
,故答案为:C6H14;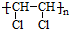 ;
;
(2)④含有碳碳三键、主链为5个C原子,名称为3,4,4-三甲基-1-戊炔,故答案为:3,4,4-三甲基-1-戊炔;
(3)甲苯苯环有5个H原子可被取代,依次编号为①②③④⑤,对应的二氯代物的氯原子位置可为①②;①③;①④;①⑤;②③;②④共6种,
TNT为三硝基甲苯,反应的化学方程式为 ,
,
故答案为:6; .
.
点评 本题考查有机物的结构与性质,为高频考点,把握物质分类、官能团、结构对称性的性质为解答的关键,注意官能团与性质的关系以及同分异构体的判断,题目难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
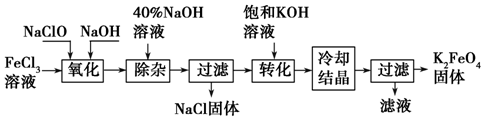
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 现象 |
| A | 加热放在坩埚中的小钠块 | 钠先熔化成光亮的小球,燃烧时,火焰为黄色,燃烧后,生成淡黄色固体 |
| B | 在酒精灯上加热铝箔 | 铝箔熔化,失去光泽,熔化的铝并不滴落,好像有一层膜兜着 |
| C | 在含有酚酞的水中加入一小块钠 | 钠浮在水面上,四处游动,发出嘶嘶响声,溶液变红 |
| D | 在空气中久置的铝条放入NaOH溶液中 | 立刻产生大量无色气泡,铝条逐渐变细,铝条逐渐发热 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
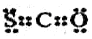
 ,可以表示35Cl-,也可以表示37Cl-
,可以表示35Cl-,也可以表示37Cl- 可以表示甲烷分子,也可以表示四氯化碳分子
可以表示甲烷分子,也可以表示四氯化碳分子
| A. | ①③⑥ | B. | ②③④⑥ | C. | ①②④⑥ | D. | 全部正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,则该分子中含有碳碳三键的数目为( )
,则该分子中含有碳碳三键的数目为( )| A. | 3 | B. | 2 | C. | 4 | D. | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题


| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的颜色不再变化 | B. | 混合气体的压强不再变化 | ||
| C. | 反应速率v(H2)=$\frac{1}{2}$v(HI) | D. | c(H2):c(I2):c(HI)=1:1:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com