
分析 已知:①N2(g)+2O2(g)═2NO2△H=+67.7kJ•mol-1
②N2H4(g)+O2(g)═N2(g)+2H2O△H=-543kJ•mol-1
③$\frac{1}{2}$H2(g)+$\frac{1}{2}$F2(g)═HF(g)△H=-269kJ•mol-1
④H2(g)+$\frac{1}{2}$O2(g)═2H2O△H=-242kJ•mol-1
(1)根据盖斯定律,②×2-①得气态肼和二氧化氮的反应,可计算出反应热,并书写热化学方程式;
(2)根据盖斯定律,③•4+②-④•2得气态肼和氟气反应的热化学方程式.
解答 解:已知:①N2(g)+2O2(g)═2NO2△H=+67.7kJ•mol-1
②N2H4(g)+O2(g)═N2(g)+2H2O△H=-543kJ•mol-1
③$\frac{1}{2}$H2(g)+$\frac{1}{2}$F2(g)═HF(g)△H=-269kJ•mol-1
④H2(g)+$\frac{1}{2}$O2(g)═2H2O△H=-242kJ•mol-1
①根据盖斯定律,②×2-①得气态肼和二氧化氮的反应的热化学方程式为2N2H4(g)+2NO2(g)═3N2(g)+4H2O(g)△H=-1153.7KJ/mol,
故答案为:2N2H4(g)+2NO2(g)═3N2(g)+4H2O(g)△H=-1153.7KJ/mol;
②根据盖斯定律,③•4+②-④•2得气态肼和氟气反应的热化学方程式为N2H4(g)+2F2 (g)═N2(g)+4HF (g)△H=-1135KJ/mol,
故答案为:N2H4(g)+2F2 (g)═N2(g)+4HF (g)△H=-1135KJ/mol.
点评 本题考查了盖斯定律在热化学方程式计算中的应用,题目难度中等,明确盖斯定律的含义及应用方法为解答关键,注意掌握热化学方程式的书写原则,试题培养了学生的分析能力及化学计算能力.


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:解答题
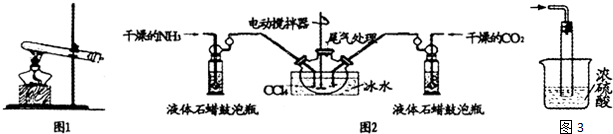
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
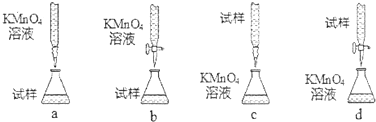
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
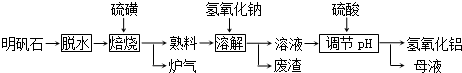
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
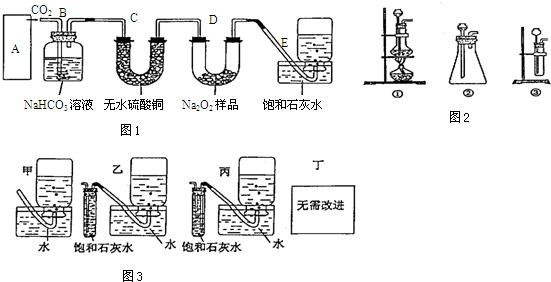
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ⅰ和Ⅱ两途径最终达到平衡时,系统内混合气体的平均相对分子质量不同 | |
| B. | Ⅰ和Ⅱ两途径最终达到平衡时,系统内混合气体的百分组成不同 | |
| C. | 达到平衡时Ⅰ途径的VA等于Ⅱ途径的VA | |
| D. | 达到平衡后,第Ⅰ途径混合气密度为第Ⅱ途径混合气密度的$\frac{1}{2}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④⑤⑥ | B. | ①②③④ | C. | ①②④⑥ | D. | ②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com