
 .
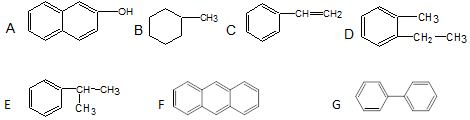
. 分析 (1)碳环化合物中含有苯环结构的化合物称为芳香芳香化合物;
仅有C、H两种元素组成的含有苯环的化合物属于芳香烃;
苯的同系物中一定含有且只含有一个苯环,其它结构一定为饱和结构且不能成环,据此进行判断;
(2)已知芳香烃A是煤焦油分馏出的一种组分.A不与溴水反应,但能使高锰酸钾酸性溶液褪色.1mol A在镍催化剂的作用下,可与3mol H2发生加成反应.0.5mol A完全燃烧,生成3.5mol CO2和2mol H2O,芳香烃A组成元素为CH,结合原子守恒1molA完全燃烧生成7mol二氧化碳和4mol水,分子式为C7H8;
解答 解:(1)A中含有苯环,属于芳香化合物,因为含有羟基,不属于烃;
B中不含有苯环,属于脂环化合物;
C中含有苯环,且只含有CH两种元素,属于芳香烃,由于含有双键,故不是苯的同系物;
D中含有1个苯环,只含有CH两种元素,且支链为烷基,属于苯的同系物;
E中含有1个苯环,只含有CH两种元素,且支链为烷基,属于苯的同系物;
F中含有3个苯环,属于芳香族化合物,且只含有CH两种元素,属于芳香烃;
G中含有2个苯环,属于芳香族化合物,且只含有CH两种元素,属于芳香烃,通过以上分析:属于芳香族化合物的是:ACDEFG; 属于芳香烃的是:CDEFG; 属于苯的同系物的是DE,
故答案为:ACDEFG;CDEFG;DE;
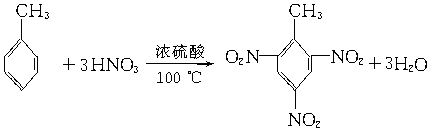
(2)1mol A在镍催化剂的作用下,可与3mol H2发生加成反应.0.5mol A完全燃烧,生成3.5mol CO2和2mol H2O,芳香烃A组成元素为CH,结合原子守恒1molA完全燃烧生成7mol二氧化碳和4mol水,分子式为C7H8,已知芳香烃A是煤焦油分馏出的一种组分.A不与溴水反应,但能使高锰酸钾酸性溶液褪色.判断A为苯的同系物甲苯,A与浓硝酸、浓硫酸混合酸在100℃时反应的化学方程式: ,
,
故答案为:甲苯; ;
;
点评 本题主要考查了有机物的分类、有机物结构、有机物性质等知识点,题目难度不大,注意通过结构特点对有机化学基础中相似概念的辨析.


科目:高中化学 来源: 题型:解答题
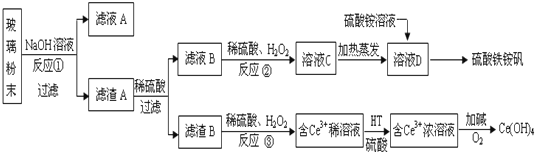
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
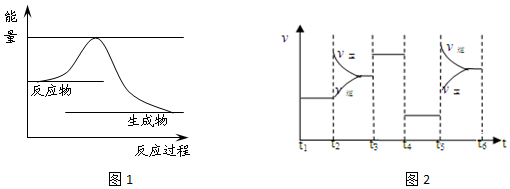
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ②③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将铜丝插入稀硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+H2O | |
| B. | 向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe═2Fe2+ | |
| C. | 向NaAlO2溶液中通入过量CO2 制Al(OH)3:CO2+AlO2-+2H2O=Al(OH)3↓+HCO3- | |
| D. | 用氨水吸收足量的SO2气体:2OH-+SO2=SO32-+H2O |
查看答案和解析>>
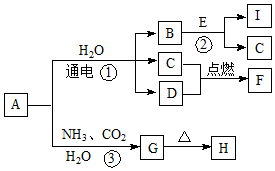
科目:高中化学 来源: 题型:推断题
 .
. 
查看答案和解析>>
科目:高中化学 来源:2017届广东省山一高三上第二次统测化学试卷(解析版) 题型:选择题
根据下列实验操作和现象得出的结论正确的是( )
选项 | 实验操作 | 现象 | 结论 |
A | 将某溶液与稀盐酸反应产生的气体通入澄清石灰水 | 石灰水变浑浊 | 该溶液中一定含有CO |
B | 将干燥的Cl2通过有色鲜花 | 鲜花褪色 | Cl2有漂白性 |
C | 向某无色溶液中滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
D | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生气体 | Na2O2没有变质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com