
下列化合物,按其晶体的熔点由高到低排列正确的是( )
A.SiC NaCl CCl4 CF4
B.SiC NaCl CF4 CCl4
C.NaCl SiC CCl4 CF4
D.CF4 CCl4 NaCl SiC
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
在通常条件下,下列各组物质的性质排列正确的是( )
A.熔点:CO2>KCl>SiO2
B.水溶性:HCl>H2S>SO2
C.沸点:乙烷>戊烷>丁烷
D.热稳定性:HF>H2O>NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
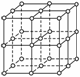
如右图,直线交点处的圆圈为NaCl晶体中Na+或Cl-所处的位置,这两种离子在空间三个互相垂直的方向上都是等距离排列的。
(1)请将其中代表Na+的圆圈涂黑(不必考虑体积大小),以完成NaCl晶体结构示意图。
(2)晶体中,在每个Na+的周围与它最接近的且距离相等的Na+共有________个。
(3)晶体中每一个重复的结构单元叫晶胞。在NaCl晶胞中正六面体的顶点上、面上、棱上的Na+或Cl-为该晶胞与其相邻的晶胞所共有,一个晶胞中Cl-的个数为________,即(填计算式)______________________;Na+的个数为________,即(填计算式)______ ___。
(4)设NaCl的摩尔质量为Mr g·mol-1,食盐晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为NA。食盐晶体中两个距离最近的钠离子中心间的距离为________________cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
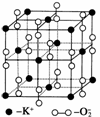
高温下,超氧化钾晶体呈立方体结构。晶体中氧的化合价部分为0价,部分为-2价。右图为超氧化钾晶体的一个晶胞,则下列说法正确的是( )
A.超氧化钾的化学式为KO2,每个晶胞中含有4个K+和4个O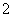
B.晶体中每个K+周围有8个O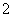 ,每个O
,每个O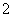 周围有8个K+
周围有8个K+
C.晶体中与每个K+距离最近且相等的K+有8个
D.晶体中0价氧与-2价氧的数目之比为5∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
有下列离子晶体空间示意图:(·阳离子,∘阴离子):
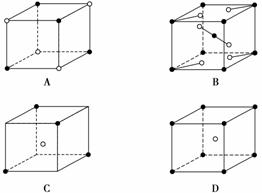
以M代表阳离子,以N表示阴离子,写出各离子晶体的组成表达式:A__________、B__________、C________、D________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是几种氯化物的熔点和沸点:
| 物质 | NaCl | MgCl2 | AlCl3 | SiCl4 |
| 熔点/℃ | 801 | 714 | 190(5×101 kPa) | -70 |
| 沸点/℃ | 1 413 | 1 412 | 180 | 57.57 |
据表中所列数据判断下列叙述与表中相吻合的是( )
A.AlCl3在加热条件下不能升华
B.SiCl4晶体属于原子晶体
C.AlCl3晶体是典型的离子晶体
D.SiCl4在晶体中有分子存在
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质中:①金属铜 ②NaOH ③I2 ④MgCl2 ⑤Na2O2 ⑥氩气
回答下列问题:
(1)不存在化学键的是________;
(2)存在金属键的是________;
(3)只存在非极性键的是________;
(4)只存在离子键的是________;
(5)既存在离子键又存在极性键的是________;
(6)既存在离子键又存在非极性键的是________;
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述不正确的是( )
A.氯化钠晶体结构为非等径圆球的密堆积
B.晶体尽量采取紧密堆积方式使其变得比较稳定
C.由于共价键有方向性和饱和性,所以原子晶体不遵循紧密堆积原则
D.金属铜和镁均以…ABAB…方式堆积
查看答案和解析>>
科目:高中化学 来源: 题型:
在形成氨气分子时,氮原子中的原子轨道发生sp3杂化生成4个________________,生成的4个杂化轨道中,只有________个含有未成对电子,所以只能与____________个氢原子形成共价键,又因为4个sp3杂化轨道有______________,所以氨气分子中的键角与甲烷不同。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com